2. tüüpi diabeedi diagnostika ja ravi
Ravijuhendi koostajad
| Mart Roosimaa (juht) | Endokrinoloog-ülemarst, SA Põhja-Eesti Regionaalhaigla; patofüsioloogia assistent, Tartu Ülikool; Eesti Endokrinoloogia Selts |
| Kaia Tammiksaar | Endokrinoloogia arst-õppejõud, SA Tartu Ülikooli Kliinikum; endokrinoloogia assistent, Tartu Ülikool; Eesti Endokrinoloogia Selts |
| Aune Rehema | Perearst, Dr Aune OÜ; meditsiinilise biokeemia kaasprofessor, Tartu Ülikool; Eesti Perearstide Selts |
| Evelin Raie | Perearst, Järveotsa Perearstikeskus; Eesti Perearstide Selts; Tallinna Perearstide Selts |
| Maarja Randväli | Diabeediõde ja toitumisterapeut, MTÜ Eesti Laste ja Noorte Diabeedi Ühing; õppejõud-assistent, Tallinna Tervishoiu Kõrgkool; MTÜ Diabeedispetsialistid |
| Anneli Vatsa | Pereõde, Tartu Kesklinna Perearstikeskus |
| Marelle Maiste | Pereõde, Ädala Perearstikeskus; Eesti Õdede Liit |
| Marko Tähnas | Partnersuhtluse osakonna juhataja, Eesti Haigekassa |
| Ulvi Tammer-Jäätes | Juhataja, Eesti Diabeediliit |
| Vallo Volke | Endokrinoloogia arst-õppejõud, SA Tartu Ülikooli Kliinikum; endokriinfüsioloogia professor, Tartu Ülikool; Eesti Endokrinoloogia Selts |
| Kärt Veliste | Ravimite ja meditsiiniseadmete osakonna peaspetsialist, Eesti Haigekassa |
| Mai Blöndal | Kardioloogia arst-õppejõud, SA Tartu Ülikooli Kliinikum; kardioloogia lektor, Tartu Ülikool |
| Urmeli Katus (juht) | Ravijuhendite metoodikanõunik, Tartu Ülikool; diabeediõde, AS Põlva Haigla; MTÜ Diabeedispetsialistid |
| Anna Vesper | Ravijuhendite metoodikanõunik, Tartu Ülikool |
| Keiu Paapsi | Nooremteadur, Tervise Arengu Instituut |
| Grit Arro | Peremeditsiini arst-resident, Tartu Ülikool |
| Helena Lepassar | Peremeditsiini arst-resident, Tartu Ülikool |
| Pille Meinson | Peaspetsialist, Eesti Maaülikool |
| Urmeli Katus | Ravijuhendite metoodikanõunik, Tartu Ülikool |
| Kairit Linnaste | Ravijuhendite metoodikanõunik, Tartu Ülikool |
| Kaja-Triin Laisaar | Ravijuhendite metoodikakonsultant, Tartu Ülikool; epidemioloogia teadur, Tartu Ülikool |
Lühendid ja mõisted
Lühendid
| ARV/ARV- ravimid |
Antiretroviirus(ravimid), ingl antiretroviral drugs |
| CI | Usaldusvahemik, ingl confidence interval |
| DPP4 inhibiitorid |
Dipeptidüül-peptidaas-4 inhibiitorid, ingl inhibitors of dipeptidyl peptidase 4 |
| eGFR | Hinnanguline glomerulaarfiltratsiooni kiirus, ingl estimated glomerular filtration rate |
| GLP1 agonistid |
Glükagoonitaolise polüpeptiidi-1 retseptori agonistid, ingl glucagon-like peptide-1 receptor agonists |
| GTT | Glükoosi taluvuse proov, ingl glucose tolerance test |
| HbA1c | Glükohemoglobiin, ingl glycated hemoglobin |
| HDL-Chol | Suure tihedusega lipoproteiin kolesterool, ingl high density lipoprotein cholesterol |
| IDF | Rahvusvaheline Diabeedi Föderatsioon, ingl International Diabetes Federation |
| IFG | Paastuglükoosi häire, ingl impaired fasting glucose |
| IGT | Glükoosi taluvuse häire, ingl impaired glucose tolerance |
| KMI | Kehamassiindeks, ingl body mass index |
| KNH | Krooniline neeruhaigus, ingl chronic kidney disease |
| LDL-Chol | Väikese tihedusega lipoproteiin kolesterool, ingl low density lipoprotein cholesterol |
| LVEF | Vasaku vatsakese väljutusfraktsioon, ingl left ventricular ejection fraction |
| MACE | Raske südame-veresoonkonna sündmus, ingl major adverse cardiovascular event |
| MODY | Monogeenne diabeet, ingl maturity onset diabetes of the young |
| OR | Šansside suhe, ingl odds ratio |
| RCT | Juhuslikustatud kontrolliga uuring, ingl randomized controlled trial |
| RJNK | Ravijuhendite nõukoda, ingl Guideline Advisory Board |
| RR | Riskide suhe, ingl relative risk |
| PICO-meetod | Patsient/sihtrühm-sekkumine-võrdlus-tulemus-näitaja, ingl Patient/Population- Intervention-Comparison-Outcome |
| SGLT2 | Naatriumist sõltuva glükoosi kaastransportija-2 inhibiitorid, ingl sodium- glucose co-transporter-2 inhibitors |
| SMBG | Vere glükoosisisalduse enesekontroll, ingl self-monitoring of blood glucose |
| SoKo/SoKo- tabel | Soovituse kokkuvõtte(tabel), ingl Evidence to Decision table |
| SVH | Südame-veresoonkonna haigus, ingl cardiovascular disease |
| TõKo/TõKo- tabel | Tõenduse kokkuvõtte(tabel), ingl Summary of Findings table |
Mõisted
| 2. tüüpi diabeet (ingl type 2 diabetes) |
Progresseeruv häire beetarakkude insuliini tootlikkuses, mis tekib sageli insuliiniresistentsuse foonil |
| Biguaniidid (ingl biguanide) |
2. tüüpi diabeedi ravis kasutatav ravimirühm, mille ainus kasutuses olev toimeaine on metformiin. Metformiini peamine toimemehhanism on glükoositootmise vähendamine maksas ja glükoosi kasutamise suurendamine perifeersetes kudedes |
| Dipeptidüül-peptidaas-4 (DPP4) inhibiitorid (ingl inhibitors of dipeptidyl peptidase-4) | 2. tüüpi diabeedi ravis kasutatav ravimirühm, mille toimel suureneb insuliini sekretsioon pankrease beetarakkudest ja väheneb glükagooni vabanemine alfarakkudest |
| Glükagoonitaolise polüpeptiidi-1 (GLP1) retseptori agonistid (ingl glucagon-like peptide-1 receptor agonists) | 2. tüüpi diabeedi ravis kasutatav ravimirühm, mille toimel suureneb insuliini sekretsioon ja väheneb glükagooni sekretsioon. GLP1 agonistid vähendavad söögiisu ja aeglustavad mao motoorikat |
| Glükohemoglobiin (HbA1c) (ingl glycated hemoglobin) |
Glükeeritud hemoglobiin ehk glükohemoglobiin moodustub, kui hemoglobiini aminorühmale lisatakse suhkrujääk. Glükohemoglobiini hulk veres on võrdelises sõltuvuses vere glükoosisisaldusega ja punaste vererakkude ehk erütrotsüütide elueaga |
| Glükoosi taluvuse häire (IGT) (ingl impaired glucose tolerance) | Paastuglükoos < 7,0 mmol/l ja vere glükoosisisaldus 2 tundi pärast glükoosilahuse joomist glükoosi taluvuse testil vahemikus ≥ 7,8 ja < 11,1 mmol/l |
| Glükoosi taluvuse proov (GTT) (ingl glucose tolerance test) | Test glükoosi ainevahetushäire tuvastamiseks. Uuringu alus on glükoosi kontsentratsioon paastuplasmas ja selle muutus 2 tundi pärast 75 g glükoosi manustamist |
| Hinnanguline glomerulaarfiltratsiooni kiirus (eGFR) (ingl estimated glomerular filtration rate) | Kasutatakse neerufunktsiooni hindamiseks või juba diagnoositud neeruhaiguse puhul neerufunktsiooni dünaamiliseks jälgimiseks. Arvutamisel arvestatakse patsiendi seerumi/ plasma kreatiniini väärtust, vanust, sugu ja rassi |
| Insuliin (ingl insulin) | Kõhunäärme beetarakkude toodetav hormoon vastusena glükoosi kontsentratsiooni suurenemisele veres. Aitab glükoosil siseneda rakkudesse, kus seda kasutatakse energia tootmiseks või salvestamiseks |
| Insuliiniresistentsus (ingl insulin resistance) |
Seisund, mille puhul ei ole keha rakud võimelised ringlevale insuliinile adekvaatselt reageerima. Tulemus on vere glükoosisisalduse suurenemine |
| Krooniline neeruhaigus (KNH) (ingl chronic kidney disease) | Üle kolme kuu kestnud neerude struktuuri või funktsiooni hälve, mille korral esineb vähemalt üks järgmistest tunnustest: albuminuuria, haiguslik leid uriini sademes, tubulaarkahjustusest tingitud elektrolüütide häire, haiguslik morfoloogiline leid, kuvamisuuringutel ilmnenud struktuurimuutus, neerusiirdamine anamneesis ja/või glomerulaarfiltratsiooni kiiruse vähenemine alla 60 mL/min/1,73 m2 (glomerulaarfiltratsiooni kiiruse astmed G3a–G5) |
| Naatriumist sõltuva glükoosi kaastransportija-2 (SGLT2) inhibiitorid (ingl sodium-glucose co- transporter-2 inhibitors) |
2. tüüpi diabeedi ravis kasutatav ravimirühm, mille toimel väheneb glükoosi renaalne tagasiimendumine ja glükoos eritub uriiniga, tuues kaasa vere glükoosisisalduse vähenemise |
| Paastuglükoosi häire (IFG) (ingl impaired fasting glucose) | Paastuglükoos 6,1–6,9 mmol/l ja vere glükoosisisaldus kaks tundi pärast glükoosilahuse joomist glükoosi taluvuse proovil < 7,8 mmol/l |
| Prediabeet (ingl prediabetes) | Prediabeet ehk eeldiabeet on seisund, mille puhul ei ole vere glükoosisisaldus diabeedi diagnoosimiseks piisavalt suur, kuid liiga suur, et pidada normaalseks. Prediabeediks peetakse paastuglükoosi häiret (IFG) ja/või glükoosi taluvuse häiret (IGT) ja/või HbA1c vahemikus 6,0%–6,4% (42–47 mmol/mol) |
| Püsiv proteinuuria (ingl persistent proteinuria) |
Viimase kolme kuu jooksul vähemalt kahes uriinianalüüsis albumiini/kreatiniini suhe > 300 mg/g või > 30 mg/mmol |
| Ravi intensiivistamine (ingl treatment intensification) |
Raviskeemi järgmise ravimirühma lisamine, et parandada glükeemilist kontrolli |
| Ravinaiivne patsient (ingl treatment naive patient) |
Patsient, kes pole varem 2. tüüpi diabeedi medikamentoosset ravi saanud |
| Vasaku vatsakese langenud väljutusfraktsioon (LVEF) (ingl reduced left ventricular ejection fraction) | LVEF-i hinnatakse ehhokardiograafiaga ja väljendatakse protsentides. Langenud väljutusfraktsiooniks peetakse LVEF-i väärtust vähem kui 40%. |
Sissejuhatus
Ravijuhendi koostamise vajadus
Diabeedi klassifikatsioon
- 1. tüüpi diabeet – pankrease beetarakkude hävimine autoimmuunreaktsiooni tõttu, mis viib tavaliselt absoluutse insuliini defitsiidini;
- 2. tüüpi diabeet – progresseeruv häire beetarakkude insuliini tootlikkuses, mis tekib sageli insuliiniresistentsuse foonil;
- gestatsioonidiabeet – raseduse ajal diagnoositud diabeet, mille puhul ei olnud tegemist enne rasedust avaldunud diabeediga;
- teised spetsiifilised tüübid – muul põhjusel tekkinud diabeeditüübid, näiteks monogeensed diabeedi sündroomid (neonataalne diabeet, MODY), pankrease haigused (tsüstiline fibroos ja pankreatiit), ravimite või kemikaalide (glükokortikosteroidid, ARV-ravimid) põhjustatud diabeet.
Diabeedi levimus Eestis
Prediabeet ja 2. tüüpi diabeedi diagnoosimine
Prediabeet ja 2. tüüpi diabeedi diagnoosimine
Prediabeet ehk eeldiabeet on seisund, mille puhul ei ole vere glükoosisisaldus nii suur, et diagnoosida diabeeti, kuid on liiga suur, et pidada normaalseks. Paastuglükoosi häireks (IFG) peetakse olukorda, kus paastuglükoos on 6,1– 6,9 mmol/l ja vere glükoosisisaldus 2 tundi pärast glükoosilahuse joomist glükoosi taluvuse proovil (GTT) < 7,8 mmol/l. Glükoosi taluvuse häire (IGT) puhul on paastuglükoos < 7,0 mmol/l ja vere glükoosisisaldus 2 tundi pärast glükoosilahuse joomist GTT-l vahemikus ≥ 7,8 ja < 11,1 mmol/l (9). Prediabeedi puhul esineb IFG ja/või IGT ja/või glükohemoglobiin (HbA1c) on vahemikus 6,0%–6,4% (42–47 mmol/mol) (9, 10).
2. tüüpi diabeet diagnoositakse kui (8–10):
- glükoosi väärtus paastuseerumis/-plasmas on ≥ 7,0 mmol/l või
- esineb hüperglükeemia sümptomaatika ja juhuslik glükoos seerumis/ plasmas on ≥ 11,1 mmol/l või
- glükoositaluvuse proovis on 2 tundi pärast 75 g glükoosi manustamist glükoosi väärtus seerumis/plasmas ≥ 11,1 mmol/l või
- HbA1c ≥ 6,5% (48 mmol/l).
Tabel 1. Glükoosi ainevahetushäire tuvastamine ja diabeedi diagnoosimine (8–10).
| Paastu- glükoos (mmol/l) |
Glükoos plasmas2 t pärast 75 g glükoosi manus- tamist (mmol/l) |
HbA1c, % (mmol/mol) |
||||
| Normaalne | ≤ 6,0 | ja | < 7,8 | ja | < 6,0 (< 42) | |
| Prediabeet |
IFG | 6,1–6,9 | ja | < 7,8 | või |
6,0–6,4 (42– 47) |
| IGT | < 7,0 | ja | 7,8–11,0 | |||
| Diabeet | ≥ 7,0 | ja/või | 11,1 | ja/või | ≥ 6,5 (≥ 48) |
- esimese astme sugulasel on diagnoositud 2. tüüpi diabeet
- suure riskiga rass / etniline taust
- anamneesis SVH
- hüpertensioon (vererõhk ≥ 140/90 mmHg või tarvitab vererõhuravimit)
- HDL-Chol < 0,90 mmol/l või triglütseriidid > 2,82 mmol/l
- polütsüstiliste munasarjade sündroom
- vähene füüsiline aktiivsus
- viited insuliiniresistentsusele
3) gestatsioonidiabeedi diagnoosiga naistel vähemalt iga kolme aasta tagant
4) HIV-iga patsientidel
5) Kõigil teistel täiskasvanutel tuleks sõelumist alustada alates 45. eluaastast. Kui vere glükoosisisaldus jääb normaalsesse vahemikku, tuleks sõeluuringut korrata vähemalt iga kolme aasta tagant.
Ravijuhendi käsitlusala ja sihtrühm
Samuti 2. tüüpi diabeedi tüsistuste ennetamine ja/või edasilükkamine, esmatasandil diabeedihaigete jälgimise suutlikkuse parandamine, eriarstiabis tehtavate põhjendamata visiitide hulga vähendamine, 2. tüüpi diabeediga seotud välditavate hospitaliseerimiste vähendamine ja diabeedipatsiendi liikumise ühtlustumine erialaspetsialistide vahel.
Ravijuhend on mõeldud kasutamiseks perearstidele ja -õdedele ning teistele tervishoiutöötajatele, kes puutuvad kokku 2. tüüpi diabeeti põdeva patsiendi raviga. Ravijuhend hõlmab prediabeediga inimesi ja 2. tüüpi diabeedi diagnoosiga patsiente alates 18. eluaastast.
Ravijuhend käsitleb riskirühma kuuluvate asümptomaatiliste inimeste sõelumist,
2. tüüpi diabeedi diagnoosimist, diagnoosiga patsiendil ravi alustamist ja -intensiivistamist, insuliinravi alustamist, ravieesmärke, vere glükoosisisalduse enesekontrolli glükomeetriga ning 2. tüüpi diabeedi diagnoosiga patsiendi jälgimist.
Ravijuhendis ei käsitleta järgmiseid teemasid:
- 1. tüüpi diabeet;
- diabeet lastel ja noortel;
- rasedusaegne diabeet;
- teised spetsiifilised diabeeditüübid (pankreatogeenne diabeet, MODY jt);
- diabeedi tüsistused ja nende ravi;
- diabeedi mittefarmakoloogiline ravi.
Ravijuhendi koostamine
Ravijuhendi koostamine
Selts. Teema võeti 2020. aasta tööplaani ning moodustati ravijuhendi töörühm ja sekretariaat (koosseisud on esitatud ravijuhendi alguses). Töörühma kaasati asjakohaste kutsealade esindajad, Eesti Haigekassa esindaja ja patsientide esindaja. Koostamise käigus kaasati konkreetsete küsimuste arutellu ka konsultandid. Eesti Haigekassa ravijuhendite nõukoda (RJNK) kinnitas töörühma liikmete koosseisu 30. märtsil 2020.
Käsitlusala lõpliku versiooni kinnitas RJNK 22. juunil 2020. Käsitlusala sisaldas
12 PICO-formaadis kliinilist küsimust ja kahte tervishoiukorralduslikku küsimust (esitatud ravijuhendi käsitlusalas). Ravijuhendi käsitlusala, täisversioon, tõenduse kokkuvõtte tabelid (TõKo), soovituste kokkuvõtte tabelid (SoKo), rakenduskava, koostajate huvide deklaratsioonide kokkuvõte ja koosolekute protokollid on kättesaadavad veebiaadressil www.ravijuhend.ee.
Ravijuhendi koostamisel lähtuti „Eesti ravijuhendite koostamise käsiraamatu 2020“ (11) põhimõtetest. Kliiniliste küsimuste arutamiseks ja soovituste sõnastamiseks, tervishoiukorralduslikele küsimustele vastamiseks ja juhendi muude materjalide (algoritmid, tabelid ja juhendi rakenduskava) arutamiseks pidas töörühm kokku kaheksa täiskoosolekut ja kolm lühikoosolekut. Peale selle toimusid koosolekute vahel töörühma liikmetega veebiarutelud. Iga koosoleku alguses vaadati läbi töörühma ja sekretariaadi liikmete võimalike huvide konfliktide deklaratsioonid ja veenduti otsustajate kallutamatuses. Koosolek oli otsustusvõimeline, kui kohal oli vähemalt 3/4 töörühma liikmetest. Koosolekute otsused olid üksmeelsed.
Soovituste koostamisel arvestati peale teadusliku tõendusmaterjali tugevuse ka sekkumise kasu tervisele (sh potentsiaalse kasu ja kahju vahekorda) ning inimeste eelistusi ja väärtushinnanguid. Samuti võeti arvesse soovitusega kaasneda võivat inimeste ebavõrdsesse olukorda jätmist ning võimalusi ja ressursse soovitatava tegevuse rakendamiseks Eestis. Enne ravijuhendi lõplikku kinnitamist retsenseerisid ravijuhendit välised eksperdid ja ravijuhend läbis avaliku tagasisideringi. Pärast kinnitamist uuendatakse ravijuhendit asjakohase teabe lisandumisel või viie aasta pärast.
Koos ravijuhendiga koostatakse patsiendimaterjal, mis käsitleb vere glükoosisisalduse enesekontrolli glükomeetriga, süstimisõpetust ja hüpoglükeemia käsitlust.
Tõendusmaterjali otsimine ja hindamine
Pärast AGREE II struktureeritud instrumendiga hindamist kaasati 2. tüüpi diabeedi ravijuhendi (RJ) töösse kuus ravijuhendit:
- American Diabetes Association. Standards of Medical Care in Diabetes – 2020. Diabetes Care 2020; 43: S1–S212.
- European Society of Cardiology and European Association for the Study of Diabetes. 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. European Heart Journal 2020; 41: 255–323.
- American Association of Clinical Endocrinologists and American College of Endocrinology. Consensus statement by the American Association of Clinical Endocrinologists and American College of Endocrinology on the comprehensive type 2 diabetes management algorithm – 2020 executive summary. Endocrine Practice 2020; 26: 107–139.
- National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. NICE; last updated 28 August 2019.
- Scottish Intercollegiate Guidelines Network. Pharmacological management of glycaemic control in people with type 2 diabetes. SIGN; 2017.
- World Health Organization. Guidelines on second- and third-line medicines and type of insulin for the control of blood glucose levels in non-pregnant adults with diabetes mellitus. WHO; 2018.
Tõendusmaterjali kokkuvõtte koostamiseks tehti lisaks süstemaatilised otsingud andmebaasis PubMed (vt otsinguprotokollid). Kaasati süstemaatilisi ülevaateid, metaanalüüse ja üksikuuringuid, eelistades jälgimisuuringutele juhuslikustatud kontrolliga katseid (RCT). Ravijuhendi koostamisel kasutatud teadusartiklid on juhendi tekstis viidatud. Sekretariaat koostas iga kliinilise küsimuse kohta TõKo tabeli ja SoKo tabeli. TõKo tabelis esitati asjakohaste teadusuuringute tulemuste kokkuvõte ja tõendatuse astme hinnang. SoKo tabelis esitati tõendusmaterjali lühikokkuvõte ning huvipakkuva tegevuse/sekkumise soovitud ja soovimatu mõju, patsientide eelistused ja väärtushinnangud, tegevuse/sekkumise vastuvõetavus ja teostatavus, ressursivajadus, kulutõhusus ning mõju tervisevõimaluste võrdsusele.
Kõik tabelid on kättesaadavad ravijuhendite veebilehel www.ravijuhend.ee.
Ravijuhendi soovituste loetelu
| Prediabeedi käsitlus | ||
| 1 | |
Prediabeediga patsient suunake eluviisisekkumise intensiivprogrammi. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
| 2 | |
Prediabeediga patsiendil ärge metformiinravi pigem kasutage. Nõrk negatiivne soovitus, mõõdukas tõendatuse aste |
| Esmase 2. tüüpi diabeedi diagnoosiga patsiendi käsitlus | ||
| 3 | |
Esmase 2. tüüpi diabeedi diagnoosiga patsiendile pakkuge intensiivset eluviisisekkumise programmi. Tugev positiivne soovitus, madal tõendatuse aste |
| 4 |
|
Esmase 2. tüüpi diabeedi diagnoosiga patsiendil, kelle HbA1c1 on ≥ 7,5% (58 mmol/mol), alustage lisaks eluviisisekkumisele farmakoteraapiaga. Tugev positiivne soovitus, madal tõendatuse aste |
| 5 |
|
Esmase 2. tüüpi diabeedi diagnoosiga patsiendile, kes ei alusta intensiivse eluviisiprogrammiga, määrake kohe farmakoteraapia. Tugev positiivne soovitus, madal tõendatuse aste |
| 6 |
|
Esmase 2. tüüpi diabeedi diagnoosiga patsiendil, kelle HbA1c on ≥ 9% (75 mmol/mol), kasutage farmakoteraapias kombinatsioonravi. Kui HbA1c on ≥ 11% (97 mmol/mol), lisage suukaudsele kombinatsioonravile insuliin.
Praktiline soovitus
|
| Farmakoteraapia alustamine 2. tüüpi diabeedi diagnoosiga patsiendil, kel puudub SVH lisarisk | ||
| 7 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kes vajab farmakoteraapiat ja kellel ei esine püsiva proteinuuriaga2 kroonilist neeruhaigust või dokumenteeritud südame vasaku vatsakese langenud väljutusfraktsiooniga3 südamepuudulikkust, alustage ravi metformiiniga. Tugev positiivne soovitus, väga madal tõendatuse aste |
| 8 |
|
2. tüüpi diabeedi diagnoosiga patsiendil alustage metformiinravi annuses vähemalt 500 mg kaks korda päevas. Vajaduse korral suurendage annust mitme nädala jooksul järk-järgult, et vähendada gastrointestinaalsete kõrvaltoimete riski. Praktiline soovitus |
| 9 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel on metformiin vastunäidustatud või kes seda ei talu, kaaluge farmakoteraapia alustamist sulfonüüluurea preparaadi, DPP4 inhibiitori, SGLT2 inhibiitori4 või pioglitasooniga. Nõrk positiivne soovitus, väga madal tõendatuse aste |
| Farmakoteraapia alustamine 2. tüüpi diabeedi diagnoosiga patsiendil, kel esineb püsiva proteinuuriaga KNH või langenud väljutusfraktsiooniga (LVEF < 40%) südamepuudulikkus | ||
| 10 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel on kaasuvana dokumenteeritud vasaku vatsakese langenud väljutusfraktsiooniga südamepuudulikkus, kaaluge farmakoteraapia alustamist SGLT2 inhibiitoriga. Nõrk positiivne soovitus, väga madal tõendatuse aste |
| 11 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel on kaasuvana püsiva proteinuuriaga krooniline neeruhaigus, kaaluge farmakoteraapia alustamist SGLT2 inhibiitoriga. Nõrk positiivne soovitus, madal tõendatuse aste |
3 Vasaku vatsakese väljutusfraktsioon (LVEF) on langenud, kui see jääb alla 40%.
4 SGLT2-inhibiitorite toime veresuhkrule sõltub glomerulaarfiltratsiooni kiirusest ja nõrgeneb oluliselt eGFR 45–60 ml/min/1,73m2 korral ning praktiliselt puudub, kui eGFR on alla 30 ml/min/1,73m2.
| Ravi esimene intensiivistamine | ||
| 12 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel ei esine püsiva proteinuuriaga kroonilist neeruhaigust, dokumenteeritud südame vasaku vatsakese langenud väljutusfraktsiooniga südamepuudulikkust või aterosklerootilist südame- veresoonkonna haigust5 ja kes senise farmakoteraapiaga ei ole saanud soovitud ravitulemust, kasutage ravi esimesel intensiivistamisel sulfonüüluurea preparaati. Tugev positiivne soovitus, madal tõendatuse aste |
| 13 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, • kellel on püsiva proteinuuriaga krooniline neeruhaigus või dokumenteeritud südame vasaku vatsakese langenud väljutusfraktsiooniga südamepuudulikkus; • kelle raviskeem ei sisalda SGLT2 inhibiitorit ja • kes senise farmakoteraapiaga ei ole saanud soovitud ravitulemust, kaaluge ravi esimesel intensiivistamisel SGLT inhibiitorit. Nõrk positiivne soovitus, madal tõendatuse aste
|
| 14 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, • kellel on püsiva proteinuuriaga krooniline neeruhaigus või dokumenteeritud südame vasaku vatsakese langenud väljutusfraktsiooniga südamepuudulikkus; • kelle raviskeem sisaldab juba SGLT2 inhibiitorit; • kes senise farmakoteraapiaga ei ole saanud soovitud ravitulemust, kasutage ravi esimesel intensiivistamisel metformiini või sulfonüüluurea preparaati. Tugev positiivne soovitus, madal tõendatuse aste
|
(2) Tserebrovaskulaarsed haigused: intratserebraalne hemorraagia (I61 koos laiendiga); peaajuinfarkt (I63 koos laiendiga); Täpsustamata kas hemorraagia või infarktitekkene insult e rabandus (I64); pretserebraalarterite peaajuinfarktita oklusioon e sulgus ja stenoos e ahenemus (I65 koos laiendiga); Peaajuarterite peaajuinfarktita oklusioon ja stenoos (I66 koos laiendiga); Insuldi (täpsustamata kas hemorraagia või infarkt) jääknähud (I69.4); (3) aordi ja perifeersete arterite aterosklerootiline kahjustus (I70 ja I71 koos laiendiga).
| 15 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, • kellel on aterosklerootiline südame-veresoonkonna haigus5; • kelle raviskeem ei sisalda SGLT2 inhibiitorit ja • kes senise farmakoteraapiaga ei ole saanud soovitud ravitulemust, kaaluge ravi esimesel intensiivistamisel SGLT inhibiitorit. Nõrk positiivne soovitus, madal tõendatuse aste
|
| Ravi teine intensiivistamine | ||
| 16 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel ei esine püsiva proteinuuriaga kroonilist neeruhaigust, dokumenteeritud südame vasaku vatsakese langenud väljutusfraktsiooniga südamepuudulikkust või aterosklerootilist südame- veresoonkonna haigust ja kes senise farmakoteraapiaga ei ole saanud soovitud ravitulemust, kasutage ravi teisel intensiivistamisel sulfonüüluureapreparaati, DPP4 inhibiitorit, pioglitasooni või SGLT2 inhibiitorit. Tugev positiivne soovitus, madal tõendatuse aste |
| 17 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, • kellel on püsiva albuminuuriaga krooniline neeruhaigus, dokumenteeritud südame vasaku vatsakese langenud väljutusfraktsiooniga südamepuudulikkus või aterosklerootiline südame- veresoonkonna haigus; • kelle raviskeem ei sisalda SGLT2 inhibiitorit ja • kes senise farmakoteraapiaga ei ole saanud soovitud ravitulemust, kasutage ravi teisel intensiivistamisel SGLT2 inhibiitorit. Tugev positiivne soovitus, madal tõendatuse aste
|
| 18 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, • kellel on püsiva proteinuuriaga kroonilineneeruhaigus, dokumenteeritud südame vasaku vatsakese langenud väljutusfraktsiooniga südamepuudulikkus või aterosklerootiline südame-veresoonkonna haigus; • kelle raviskeem sisaldab juba SGLT2 inhibiitorit või selle kasutamine on vastunäidustatud ja • kes senise farmakoteraapiaga ei ole saavutanud soovitud ravitulemust, kaaluge ravi teisel intensiivistamisel GLP1 agonisti. Nõrk positiivne soovitus, madal tõendatuse aste
|
| Ravi kolmas intensiivistamine | ||
| 19 |
|
2. tüüpi diabeedi diagnoosiga patsiendil kaaluge ravi kolmandal intensiivistamisel basaalinsuliini või GLP1 agonisti. Nõrk positiivne soovitus, väga madal tõendatuse aste |
| Kroonilise neeruhaiguse või vasaku vatsakese langenud väljutusfraktsiooniga (LVEF < 40%) südamepuudulikkuse ja 2. tüüpi diabeedi diagnoosiga patsiendi käsitlus | ||
| 20 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel on kaasuvana dokumenteeritud vasaku vatsakese langenud väljutusfraktsiooniga südamepuudulikkus, kaaluge raviskeemi SGLT2 inhibiitori lisamist olenemata HbA1c väärtusest. Nõrk positiivne soovitus, mõõdukas tõendatus |
| 21 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel on püsiva proteinuuriaga krooniline neeruhaigus, kaaluge raviskeemi SGLT2 inhibiitori lisamist olenemata HbA1c väärtusest. Nõrk positiivne soovitus, mõõdukas tõendatuse aste |
| Ravi eesmärkväärtused | ||
| 22 | |
2. tüüpi diabeedi diagnoosiga patsiendil hinnake ravimotivatsiooni ja -tulemusi vähemalt kaks korda aastas. Praktiline soovitus |
| 23 | |
2. tüüpi diabeedi diagnoosiga patsiendil seadke HbA1c eesmärkväärtuseks < 7,0% (53 mmol/mol). Tugev positiivne soovitus, madal tõendatuse aste |
| 24 |
|
Eluviisiprogrammis osaleval või metformiini monoteraapial oleval patsiendil, kellel pole diabeedi kaugtüsistusi ega varem diagnoositud südame-veresoonkonna haigust, kaaluge HbA1c eesmärkväärtust < 6,5% (48 mmol/mol). Nõrk positiivne soovitus, madal tõendatuse aste |
| 25 |
|
Kauakestnud 2. tüüpi diabeediga, väljendunud hilistüsistustega, raskete kaasuvate haigustega või varem raskeid hüpoglükeemiaid läbi teinud patsiendil kaaluge vähem rangeid HbA1c eesmärkväärtuseid (< 8,0%, 64 mmol/ mol). Nõrk positiivne soovitus, madal tõendatuse aste |
| 26 | |
2. tüüpi diabeedi diagnoosiga patsiendil kasutage glükeemilise kontrolli hindamisel lisaks HbA1c-le glükoosi väärtuseid. Praktiline soovitus |
| Vere glükoosisisalduse glükomeetriga enesekontroll patsientidel, kelle raviskeem ei sisalda insuliini | ||
| 27 |
|
2. tüüpi diabeedi diagnoosiga patsiendile, kes ei saa insuliinravi, ärge regulaarset enesekontrolli glükomeetriga soovitage. Tugev negatiivne soovitus, mõõdukas tõendatuse aste |
| 28 |
|
2. tüüpi diabeedi diagnoosiga patsiendile, kes ei saa insuliinravi, soovitage enesekontrolli glükomeetriga üksnes vajaduse korral (nt muutus raviskeemis, enne õe või arsti vastuvõttu, hüpoglükeemia kahtlusel). Tugev positiivne soovitus, mõõdukas tõendatuse aste |
| Vere glükoosisisalduse glükomeetriga enesekontroll patsientidel, kelle raviskeem sisaldab insuliini | ||
| 29 |
|
2. tüüpi diabeedi diagnoosiga patsiendile, kelle farmakoloogiline ravi sisaldab insuliini, soovitage vere glükoosisisalduse glükomeetriga kontrollimist hüpoglükeemia kahtluse korral ja pärast madala glükoositaseme korrigeerimist, enne tähelepanu nõudvate tegevuste (nt masinatega töötamine või mootorsõiduki juhtimine) sooritamist ja nende ajal ning ägeda haiguse korral (nt palavik > 38 °C, infektsioon). Praktiline soovitus |
| 30 |
|
2. tüüpi diabeedi diagnoosiga patsiendile, kelle raviskeem sisaldab ainult basaalinsuliini, soovitage vere glükoosisisalduse kontrollimist glükomeetriga enne hommikusööki ravi alustamisel või annuse muutmisel. Tugev positiivne soovitus, väga madal tõendatuse aste |
| 31 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kelle raviskeem sisaldab ainult basaalinsuliini, kaaluge vere glükoosisisalduse kontrollimist glükomeetriga üks kord kuus 3–4 korda päevas. Tugev positiivne soovitus, väga madal tõendatuse aste |
| 32 |
|
2. tüüpi diabeedi diagnoosiga patsiendile, kes on insuliini mitmesüsteravil, soovitage vere glükoosisisalduse kontrollimist glükomeetriga 3–4 korda päevas (nt enne põhitoidukordi ja magamaminekut). Tugev positiivne soovitus, väga madal tõendatuse aste |
| 33 |
|
2. tüüpi diabeedi diagnoosiga patsiendile, kes on insuliinravil, õpetage koos vere glükoosisisalduse enesemonitooringuga glükoosi näidu järgi insuliini annuse korrigeerimist. Praktiline soovitus |
| Patsiendi suunamine eriarstiabisse | ||
| 34 |
|
2. tüüpi diabeedi diagnoosiga patsient, kellel on dekompenseerunud diabeet või vajalik alustada insuliinravi, kaaluge endokrinoloogi vastuvõtule suunamist. Praktiline soovitus |
| 35 |
|
2. tüüpi diabeedi diagnoosiga patsient, kellel kahtlustate muud spetsiifilist diabeedi vormi, suunake endokrinoloogi vastuvõtule. Praktiline soovitus |
| 36 | |
2. tüüpi diabeedi diagnoosiga insuliinravil olev patsient suunake vähemalt üks kord aastas diabeediõe vastuvõtule. Praktiline soovitus |
| 37 |
|
2. tüüpi diabeedi diagnoosiga patsient, kes vajab spetsiifilist eluviisinõustamist (sh senine nõustamine olnud vähetõhus, esinevad kaasuvad haigused nt podagra, krooniline neerupuudulikkus, hüperkolesteroleemia, tsöliaakia jt), suunake diabeediõe või toitumisterapeudi vastuvõtule. Praktiline soovitus |
| 38 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kes on kehamassiindeksiga vähemalt 35 kg/m2, kaaluge ravijuhendi „Bariaatrilise patsiendi käsitlus enne ja pärast kirurgilist sekkumist“ põhjal üldkirurgi vastuvõtule suunamist. Praktiline soovitus |
| 39 |
|
2. tüüpi diabeedi diagnoosiga patsient, kes planeerib rasedust, suunake endokrinoloogi, naistearsti või rasedatega tegeleva sisearsti konsultatsioonile. Praktiline soovitus |
| 40 |
|
2. tüüpi diabeedi diagnoosiga patsient, kes on rasestunud, suunake endokrinoloogi, naistearsti või rasedatega tegeleva sisearsti konsultatsioonile ühe nädala jooksul. Praktiline soovitus |
Ravijuhendi soovitused koos tõenduse ja arutelu lühikokkuvõttega
Prediabeedi käsitlus
Prediabeedi käsitlus
Eesti ravijuhend „Ülekaalulise või rasvunud patsiendi käsitlus esmatasandil“ (2019) ütleb, et eluviisi nõustamine on eluviisi, sh toitumis- ja liikumisharjumuste muutmine, milleks kasutatakse eri sekkumisi (13). 2. tüüpi diabeedi ennetamiseks ja/või edasilükkamiseks võib kasutada nii eluviisisekkumisi kui ka farmakoteraapiat. Mitu suurt juhuslikustatud kontrolliga katset (RCT) (sh The Diabetes Prevention Program, The Finnish Diabetes Prevention Study ja The DaQing Diabetes Prevention Study) on uurinud eluviisisekkumiste mõju 2. tüüpi diabeedi ennetamisele (14–16). Farmakoteraapia kasutamisest 2. tüüpi diabeedi ennetamisel on kõige rohkem tõendust metformiini kohta (17).
| 1 | Prediabeediga patsient suunake eluviisisekkumise intensiivprogrammi. Tugev positiivne soovitus, mõõdukas tõendatuse aste |
|
| 2 | Prediabeediga patsiendil ärge metformiinravi pigem kasutage. Nõrk negatiivne soovitus, mõõdukas tõendatuse aste |
Töörühm võttis soovituse sõnastamisel arvesse, et inimesed, kes osalevad eluviisisekkumise programmides, on tõenäoliselt keskmisest motiveeritumad. Enamik prediabeediga patsiente on nõus oma eluviisis midagi muutma. Intensiivse eluviisisekkumise potentsiaalsed soovimatud mõjud on vaimne pinge ja olemasoleva toitumishäire võimendumine (kahtlusel tuleb selle suhtes sõeluda). Farmakoteraapias kasutatakse valdavalt metformiini. Metformiini väga sage kõrvaltoime on seedetrakti ärritus, nagu iiveldus, oksendamine, kõhulahtisus, kõhuvalu ja söögiisu kaotus. Need kõrvaltoimed esinevad kõige sagedamini ravi alustamisel ja enamikul juhtudel lahenevad spontaanselt. Ravi metformiiniga on uuritud peamiselt 2. tüüpi diabeedi ennetamisel. Mõju suremusele ja SV tulemitele enamasti hinnatud ei ole. Kuigi metformiinravi vähendab veresuhkru taset ja esmashaigestumist 2. tüüpi diabeeti, puudub tõestatud mõju teistele kliiniliselt olulistele tulemusnäitajatele, sh südame-veresoonkonnale.
Vaata lähemalt kliinilise küsimuse number 1 TõKo tabelit ja SoKo tabelit.
Esmase 2. tüüpi diabeedi diagnoosiga patsiendi käsitlus
| 3 | |
Esmase 2. tüüpi diabeedi diagnoosiga patsiendile pakkuge intensiivset eluviisisekkumise programmi. Tugev positiivne soovitus, madal tõendatuse aste |
| 4 |
|
Esmase 2. tüüpi diabeedi diagnoosiga patsiendil, kelle HbA1c6 on ≥ 7,5% (58 mmol/mol), alustage lisaks eluviisisekkumisele farmakoteraapiaga. Tugev positiivne soovitus, madal tõendatuse aste |
| 5 |
|
Esmase 2. tüüpi diabeedi diagnoosiga patsiendile, kes ei alusta intensiivse eluviisiprogrammiga, määrake kohe farmakoteraapia. Tugev positiivne soovitus, madal tõendatuse aste |
8 Glükohemoglobiini (HbA1c) kasutatakse diabeedi diagnoosimiseks ja haiguskulu jälgimiseks. HbA1c hulk veres on otseses seoses vere glükoosisisalduse ja erütrotsüütide elueaga (keskmiselt 120 päeva).
| 6 |
|
Esmase 2. tüüpi diabeedi diagnoosiga patsiendil, kelle HbA1c on ≥ 9% (75 mmol/mol), kasutage farmakoteraapias kombinatsioonravi. Kui HbA1c on ≥ 11% (97 mmol/mol), lisage suukaudsele kombinatsioonravile insuliin. Praktiline soovitus |
Töörühm võttis soovituste sõnastamisel arvesse, et kuigi hetkel puudub Eestis intensiivne eluviisisekkumise programm, kuhu patsient suunata, tuleb tõendusest lähtuvalt anda positiivne soovitus selle kasutamiseks. Intensiivse eluviisisekkumise programmi loomise algatus fikseeritakse ühe rakendustegevusena. Töörühm oli seisukohal, et eluviisisekkumist peavad läbi viima väljaõppe saanud spetsialistid. Töörühm võttis soovituste tugevuse astme tõstmisel arvesse, et kuna intensiivne eluviisisekkumine (füüsiline aktiivsus koos samaaegse toitumisalase interventsiooniga) langetas HbA1c-d keskmiselt kuni 1% võrra, tuleb HbA1c ≥ 7,5% korral (58 mmol/mol) alustada lisaks farmakoteraapiaga. Patsiendid, kellel ei ole seoses kaasuvate haigustega võimalik intensiivses eluviisiprogrammis osaleda või ei ole selleks motiveeritud, peaksid kohe alustama farmakoteraapiaga. 2. tüüpi diabeedi diagnoosiga patsientidele, kes ei saanud või ei soovinud kohe pärast diabeedi diagnoosimist eluviisisekkumise programmiga alustada, tuleks seda võimalust korduvalt pakkuda. Eluviisisekkumise peamised ebasoodsad mõjud on vigastuse ja ülekoormuse risk, rasvunud inimestel võivad tekkida luu- ja liigeseprobleemid, olemasoleva toitumishäirega inimestel haiguse ägenemine (kahtluse korral tuleb selle suhtes sõeluda). Kontrollitud tingimustes on eluviisisekkumise potentsiaalne soovimatu mõju väike, kuid soovitud mõju suur. Lisaks püsib eluviisisekkumise positiivne mõju võrreldes farmakoteraapiaga kauem. Diabeedi eri suukaudsed ravimirühmad langetavad monoteraapiana HbA1c-d 0,6–0,9% võrra, seetõttu tuleks kõrgema HbA1c väärtuse korral ravimirühmi juba ravi alustamisel kombineerida.
Vaata lähemalt kliinilise küsimuse number 2 TõKo tabeleid 1–3 ja SoKo tabelit.
Farmakoloogilise ravi alustamine ravinaiivsel 2. tüüpi diabeedi diagnoosiga patsiendil
SVH lisariskita ravinaiivne 2. tüüpi diabeedi diagnoosiga patsient
| 7 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kes vajab farmakoteraapiat ja kellel ei esine püsiva proteinuuriaga7 kroonilist neeruhaigust või dokumenteeritud südame vasaku vatsakese langenud väljutusfraktsiooniga8 südamepuudulikkust, alustage ravi metformiiniga. Tugev positiivne soovitus, väga madal tõendatuse aste |
| 8 |
|
2. tüüpi diabeedi diagnoosiga patsiendil alustage metformiinravi annuses vähemalt 500 mg kaks korda päevas. Vajaduse korral suurendage annust mitme nädala jooksul järk-järgult, et vähendada gastrointestinaalsete kõrvaltoimete riski. Praktiline soovitus |
| 9 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel on metformiin vastunäidustatud või kes seda ei talu, kaaluge farmakoteraapia alustamist sulfonüüluurea preparaadi, DPP4 inhibiitori, SGLT2 inhibiitori9 või pioglitasooniga. Nõrk positiivne soovitus, väga madal tõendatuse aste |
Töörühm võttis soovituse sõnastamisel arvesse, et kõik ravimirühmad langetavad võrreldes platseeboga oluliselt HbA1c-d ja farmakoteraapia alustamisel tuleb valida ravimirühmadest üks. Soovituse tugevuse tõstmisel võeti arvesse, et metformiini soovitamine esmavalikuna ei kahjusta patsienti. Kuigi metformiini väga sage kõrvaltoime on seedetrakti ärritus, esineb see kõige sagedamini ravi alustamisel ja enamikul juhtudel laheneb spontaanselt. Suurema annusega alustamisel on ka suurem risk seedetrakti ärrituseks. Metformiin on kehakaaluneutraalne ja ei suurenda monoteraapiana hüpoglükeemia riski. Metformiini on kliinilises praktikas kaua kasutatud ja see on ravimirühmadest kõige odavam (sh väikseim omaosalus). Metformiin on suukaudne ravim, mis võrreldes süstitavaga võiks olla sihtrühmale vastuvõetavam. Risk ebasoodsateks tulemiteks (raske hüpoglükeemia, suremus, infarkt ja insult) ja ravimirühmade mõju HbA1c-le ei erinenud ravimirühmade vahel, seetõttu ei piiratud ravimirühmade valikut metformiini sobimatuse korral.
Vaata lähemalt kliinilise küsimuse number 3 soovituse TõKo tabeleid 1 ja 2 ning SoKo tabelit.
Püsiva proteinuuriaga või vasaku vatsakese langenud väljutusfraktsiooniga (LVEF < 40%) südamepuudulikkusega 2. tüüpi diabeedi diagnoosiga patsient
2. tüüpi diabeet on südame isheemiatõve, insuldi ja SV põhjustest tingitud suremuse iseseisev riskitegur, mis suurendab riski keskmiselt kaks korda (36). Lisaks heale glükeemilisele kontrollile on oluline, et diabeediravim ise ei suurendaks SVH riski. Pikalt kasutusel olnud diabeediravimite, nagu metformiin, sulfonüüluuread, glitasoonid ja insuliin, mõju südame-veresoonkonnale ei ole hinnatud suurtes RCT-des, nagu seda on tehtud hiljem turule tulnud preparaatide puhul, sh DPP4 inhibiitorid, SGLT2 inhibiitorid ja GLP1 agonistid (27). Esimest korda on olemas tulemused suurtest RCT-dest, mis viitavad SGLT2 inhibiitorite (EMPAREG, CANVAS program, DECLARE TIMI 58, CREDENCE, VERTIS- CV, DAPA-HF, EMPEROR-REDUCED, DAPA CKD, SCORED, SOLOIST WHF) (37–46) ja GLP1 agonistide (ELIXA, LEADER, SUSTAIN-6, EXSCEL, HARMONY, REWIND, PIONEER 6) (47–53) kardio- ja nefroprotektiivsele mõjule.
| 10 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel on kaasuvana dokumenteeritud vasaku vatsakese langenud väljutusfraktsiooniga südamepuudulikkus, kaaluge farmakoteraapia alustamist SGLT2 inhibiitoriga. Nõrk positiivne soovitus, väga madal tõendatuse aste |
| 11 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel on kaasuvana püsiva proteinuuriaga krooniline neeruhaigus, kaaluge farmakoteraapia alustamist SGLT2 inhibiitoriga. Nõrk positiivne soovitus, madal tõendatuse aste |
Töörühm võttis soovituse andmisel arvesse tõendust SGLT2 inhibiitorite kohta kliinilise küsimuse nr 8 alt, mis pärines suurtest RCT-dest, (37–46) ja samu uuringuid kaasanud süstemaatilistest ülevaadetest ja metaanalüüsidest.
SGLT2 inhibiitoritel oli võrreldes platseeboga väiksem suremuse, raske südameveresoonkonna sündmuse (MACE), südamepuudulikkuse pärast hospitaliseerimise ja neerudega seotud negatiivsete tulemite risk (65). Töörühm jagas patsientide sihtrühma neljaks alarühmaks: suure või väga suure SVH riskiga patsiendid (sihtorgani kahjustus või mitu riskifaktorit), aterosklerootilise SVH-ga patsiendid, dokumenteeritud vasaku vatsakese langenud väljutusfraktsiooniga (LVEF < 40%) südamepuudulikkusega patsiendid ja püsiva proteinuuriaga KNH-ga patsiendid. Töörühm jõudis järeldusele, et praegu pole piisavalt tõendust soovitamaks suure või väga suure SVH riskiga või aterosklerootilise SVH-ga patsientidel ravi alustamist SGLT2 inhibiitoritega. Tõendus 2. tüüpi diabeedi ja langenud LVEF südamepuudulikkusega patsientide kohta kliinilisest küsimusest nr 8 oli kaudne ja pärines peamiselt kahest südamepuudulikkusega patsiente uurinud RCT-st DAPA HF ja EMPEROR REDUCED, kus vastavalt 49,8%-l ja 67,5%-l patsientidest oli kaasuvana ka 2. tüüpi diabeet. Uuringutes oli tegu platseebovõrdlusega (meid huvitas selle küsimuse all võrdlus metformiiniga) ja kombinatsioonraviga (meid huvitas monoteraapia). Tõendus SGLT2 inhibiitorite kasutamisest 2. tüüpi diabeedi ja KNH-ga patsientidel kliinilisest küsimusest nr 8 oli kaudne ja pärines kahest 2. tüüpi diabeedi uuringust (CREDENCE ja SCORED), kuhu kaasati ainult KNH-ga patsiendid, ja ühest KNH uuringust, kus 67,5%-l uuritavatest oli kaasuvana 2. tüüpi diabeet. Lisaks oli teistesse diabeediuuringutesse kaasatud neeruhaigusega patsiente: EMPAREG, CANVAS ja VERTIS CV kaasasid patsiente, kelle eGFR oli vähemalt 30 ml/min/1,73m2; DECLARE TIMI patsiente, kelle eGFR oli vähemalt 60 ml/min/1,73m2. Uuringutes oli tegu platseebovõrdlusega ja kombinatsioonraviga.
Töörühm võttis soovituse sõnastamisel arvesse, et Palmeri et al. (2021) süstemaatilise ülevaate ja võrgustik-metaanalüüsi põhjal (66) oli SGLT2 inhibiitorite ja GLP1 agonistide kardio- ja nefroprotektiivne mõju sarnane. Kuna GLP1 agonistide hind (sh omaosalus) on võrreldes SGLT2 inhibiitoritega 2 korda suurem, ei ole GLP1 agonisti kasutamine ravi alustamisel põhjendatud.
Vaata lähemalt kliinilise küsimuse number 4 Tõko ja Soko tabelit.
Ravi intensiivistamine
Ravi esimene ja teine intensiivistamine
| 12 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel ei esine püsiva proteinuuriaga kroonilist neeruhaigust, dokumenteeritud südame vasaku vatsakese langenud väljutusfraktsiooniga südamepuudulikkust või aterosklerootilist südame- veresoonkonna haigust5 ja kes senise farmakoteraapiaga ei ole saanud soovitud ravitulemust, kasutage ravi esimesel intensiivistamisel sulfonüüluurea preparaati. Tugev positiivne soovitus, madal tõendatuse aste |
| 13 |
|
2. tüüpi diabeedi diagnoosiga patsiendil,
Nõrk positiivne soovitus, madal tõendatuse aste |
14 |
|
2. tüüpi diabeedi diagnoosiga patsiendil,
Tugev positiivne soovitus, madal tõendatuse aste |
| 15 |
|
2. tüüpi diabeedi diagnoosiga patsiendil,
Nõrk positiivne soovitus, madal tõendatuse aste |
Tõsiste kõrvaltoimete šanss ravimite kombinatsioonide vahel ei erinenud (67– 78). Võrreldes platseebo lisamisega vähenes SV suremuse, müokardiinfarkti, neeru- ja südamepuudulikkuse tõttu hospitaliseerimise risk, kui raviskeemi lisati SGLT2 inhibiitor. SV suremuse, müokardiinfarkti, neerupuudulikkuse ja insuldi risk oli väiksem, kui raviskeemi lisati GLP1 agonist, võrreldes sellega, kui lisati platseebo. Mõju oli suurem SVH riski suurenedes (66).
Töörühm võttis soovituse tugevuse tõstmisel arvesse, et sulfonüüluurea soovitamine ei kahjusta patsienti. Sulfonüüluuread on kauaaegse kasutuskogemuse ja väiksese omaosalusega ravimirühm. Töörühm võttis soovituse sõnastamisel arvesse tõendust SGLT2 inhibiitorite kohta kliinilise küsimuse nr 8 alt, mis pärines suurtest RCT- dest (37–46), ning neid samu uuringuid kaasavatest süstemaatilistest ülevaadetest ja metaanalüüsidest. Eelmainitud uuringud kaasasid ka aterosklerootilise SVH või selle riskiga patsiente. Uuringute tulemused viitasid, et kardioprotektiivne mõju võiks olla ka juba SVH riskiga patsientidel. Samas oli Palmeri et al. (2021) süstemaatilise ülevaate ja võrgustik-metaanalüüsi põhjal (66) oli SGLT2 inhibiitorite ja GLP1 agonistide kardio- ja nefroprotektiivne mõju sarnane. Kuna GLP1 agonistide hind (sh omaosalus) on võrreldes SGLT2 inhibiitoritega u 2 korda suurem, ei ole GLP1 agonisti kasutamine ravi esimesel intensiivistamisel põhjendatud.
Vaata lähemalt kliinilise küsimuse nr 5 TõKo tabeleid 1–4 ja SoKo tabelit.
Vaata lähemalt kliinilise küsimuse nr 8 TõKo tabeleid 1–8 ja SoKo tabelit.
| 16 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel ei esine püsiva proteinuuriaga kroonilist neeruhaigust, dokumenteeritud südame vasaku vatsakese langenud väljutusfraktsiooniga südamepuudulikkust või aterosklerootilist südame- veresoonkonna haigust ja kes senise farmakoteraapiaga ei ole saanud soovitud ravitulemust, kasutage ravi teisel intensiivistamisel sulfonüüluureapreparaati, DPP4 inhibiitorit, pioglitasooni või SGLT2 inhibiitorit. Tugev positiivne soovitus, madal tõendatuse aste |
| 17 |
|
2. tüüpi diabeedi diagnoosiga patsiendil,
Tugev positiivne soovitus, madal tõendatuse aste |
| 18 |
|
2. tüüpi diabeedi diagnoosiga patsiendil,
Nõrk positiivne soovitus, madal tõendatuse aste |
Vaata lähemalt kliinilise küsimuse nr 6 TõKo tabeleid 1 ja 2 ning SoKo tabelit.
Vaata lähemalt kliinilise küsimuse nr 8 TõKo tabeleid 1–8 ja SoKo tabelit.
Vaata lähemalt kliinilise küsimuse nr 9 TõKo ja SoKo tabelit.
Ravi kolmas intensiivistamine
| 19 |
|
2. tüüpi diabeedi diagnoosiga patsiendil kaaluge ravi kolmandal intensiivistamisel basaalinsuliini või GLP1 agonisti. Nõrk positiivne soovitus, väga madal tõendatuse aste |
Vaata lähemalt kliinilise küsimuse nr 7 SoKo tabelit.
SGLT2 inhibiitori kasutamine kroonilise neeruhaiguse või langenud väljutusfraktsiooniga (LVEF < 40%) südamepuudulikkuse ja 2. tüüpi diabeedi diagnoosiga patsiendi ravis
| 20 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel on kaasuvana dokumenteeritud vasaku vatsakese langenud väljutusfraktsiooniga südamepuudulikkus, kaaluge raviskeemi SGLT2 inhibiitori lisamist olenemata HbA1c väärtusest. Nõrk positiivne soovitus, mõõdukas tõendatus |
| 21 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kellel on püsiva proteinuuriaga krooniline neeruhaigus, kaaluge raviskeemi SGLT2 inhibiitori lisamist olenemata HbA1c väärtusest. Nõrk positiivne soovitus, mõõdukas tõendatuse aste |
Töörühm võttis arvesse, et 2. tüüpi diabeediga patsientidel, kelle raviskeemi lisatakse SGLT2 inhibiitor kardio- ja/või nefroprotektiivsetel eesmärkidel, võib tekkida hüpoglükeemia risk. Seetõttu tuleb SGLT2 inhibiitori sellel eesmärgil lisamisel üle vaadata teiste raviskeemis olevate antidiabeetiliste ravimitega jätkamise vajadus.
Vaata lähemalt kliinilise küsimuse nr 8 TõKo tabeleid 1–8 ja SoKo tabelit.
Ravi eesmärkväärtused
| 22 | |
2. tüüpi diabeedi diagnoosiga patsiendil hinnake ravimotivatsiooni ja -tulemusi vähemalt kaks korda aastas. Praktiline soovitus |
| 23 | |
2. tüüpi diabeedi diagnoosiga patsiendil seadke HbA1c eesmärkväärtuseks < 7,0% (53 mmol/mol). Tugev positiivne soovitus, madal tõendatuse aste |
| 24 |
|
Eluviisiprogrammis osaleval või metformiini monoteraapial oleval patsiendil, kellel pole diabeedi kaugtüsistusi ega varem diagnoositud südame-veresoonkonna haigust, kaaluge HbA1c eesmärkväärtust < 6,5% (48 mmol/mol). Nõrk positiivne soovitus, madal tõendatuse aste |
| 25 |
|
Kauakestnud 2. tüüpi diabeediga, väljendunud hilistüsistustega, raskete kaasuvate haigustega või varem raskeid hüpoglükeemiaid läbi teinud patsiendil kaaluge vähem rangeid HbA1c eesmärkväärtuseid (< 8,0%, 64 mmol/ mol). Nõrk positiivne soovitus, madal tõendatuse aste |
| 26 | |
2. tüüpi diabeedi diagnoosiga patsiendil kasutage glükeemilise kontrolli hindamisel lisaks HbA1c-le glükoosi väärtuseid. Praktiline soovitus |
Töörühm võttis soovituse sõnastamisel arvesse, et igapäevatöös kasutatakse glükeemilise kontrolli hindamiseks kõige rohkem HbA1c-d. Töörühm võttis soovituse tugevuse suurendamisel arvesse, et kõigil, kellel on võimalik seda ilma soovimatute mõjudeta saavutada, tuleks eelistada väiksemaid eesmärkväärtuseid. Intensiivsete eesmärkväärtuste peamine soovimatu mõju on hüpoglükeemiad.
Samas ei võrdu intensiivne kontroll automaatselt suurema hüpoglükeemia riskiga. Ka kehva glükeemilise kontrolli puhul võib esineda sagedast hüpoglükeemiat. Suurim hüpoglükeemia risk kaasneb insuliinraviga. Intensiivsete eesmärkväärtuste seadmisel on tervishoiutöötaja kohustus patsienti nõustada, kuidas hüpoglükeemiat ennetada, ära tunda ja ravida. Insuliinravil intensiivse kontrolli saavutamine nõuab vere glükoosisisalduste sagedast mõõtmist, mis ei pruugi olla kõigile inimestele vastuvõetav.
Vaata lähemalt kliinilise küsimuse nr 10 TõKo tabeleid 1–3 ja SoKo tabelit.
Vere glükoosisisalduse enesekontroll glükomeetriga
SMBG) on oluline osa 2. tüüpi diabeeti põdevate ja insuliinravil olevate patsientide ravis (100, 101). Seevastu ei pea teisi antidiabeetilisi ravimeid kasutavad patsiendid vere glükoosisisaldust hindama, et selle järgi võetava ravimi annust muuta. Kapillaarverest tehtud mõõtmine suurendab insuliinravil mitteolevate patsientide teadlikkust sellest, kuidas eri tegurid (toidu kogus ja toitaineline jaotus, füüsiline aktiivsus jms) mõjutavad vere glükoosisisaldust, aidates kaasa positiivsetele ja püsivatele elustiilimuutustele. Igapäevase mõõtmise dokumenteerimine aitab tervishoiutöötajal individuaalset raviplaani koostada ja seda kohandada, näiteks ravimite väljakirjutamisel (kas patsient vajab pigem paastuglükoosi või toidukorrajärgse glükoosisisalduse korrigeerimist) (101, 103). Toidukorrajärgne glükoositaseme jälgimine (mida saab teha ainult SMBG kaudu) on üks peamiseid viise diabeedi kontrolli all hoidmiseks (104). Vere glükoositaseme enesekontroll aitab õige kasutuse korral patsienti võimestada ja tal diabeediga paremini toime tulla, toetada tervishoiutöötajaid individuaalsete soovituste andmisel ja raviskeemi korrigeerimisel. Samas võib üleliigne mõõtmine põhjustada patsiendile liigset stressi ja muret. SMBG on eriti oluline nende patsientide puhul, kelle raviskeem sisaldab insuliini (105, 106).
Vere glükoosisisalduse enesekontroll glükomeetriga patsientidel, kelle raviskeem ei sisalda insuliini
| 27 |
|
2. tüüpi diabeedi diagnoosiga patsiendile, kes ei saa insuliinravi, ärge regulaarset enesekontrolli glükomeetriga soovitage. Tugev negatiivne soovitus, mõõdukas tõendatuse aste |
| 28 |
|
2. tüüpi diabeedi diagnoosiga patsiendile, kes ei saa insuliinravi, soovitage enesekontrolli glükomeetriga üksnes vajaduse korral (nt muutus raviskeemis, enne õe või arsti vastuvõttu, hüpoglükeemia kahtlusel). Tugev positiivne soovitus, mõõdukas tõendatuse aste |
Töörühm võttis soovituse sõnastamisel arvesse, et SMBG saavutatud vähenenud HbA1c oli kliiniliselt pigem mitteoluline. Samas on SMBG tähtis ravivastuse hindamisel.
Vaata lähemalt kliinilise küsimuse nr 11 TõKo ja SoKo tabelit.
Vere glükoosisisalduse enesekontroll glükomeetriga patsientide puhul, kelle raviskeem sisaldab insuliini
| 29 |
|
2. tüüpi diabeedi diagnoosiga patsiendile, kelle farmakoloogiline ravi sisaldab insuliini, soovitage vere glükoosisisalduse glükomeetriga kontrollimist hüpoglükeemia kahtluse korral ja pärast madala glükoositaseme korrigeerimist, enne tähelepanu nõudvate tegevuste (nt masinatega töötamine või mootorsõiduki juhtimine) sooritamist ja nende ajal ning ägeda haiguse korral (nt palavik > 38 °C, infektsioon). Praktiline soovitus |
| 30 |
|
2. tüüpi diabeedi diagnoosiga patsiendile, kelle raviskeem sisaldab ainult basaalinsuliini, soovitage vere glükoosisisalduse kontrollimist glükomeetriga enne hommikusööki ravi alustamisel või annuse muutmisel. Tugev positiivne soovitus, väga madal tõendatuse aste |
| 31 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kelle raviskeem sisaldab ainult basaalinsuliini, kaaluge vere glükoosisisalduse kontrollimist glükomeetriga üks kord kuus 3–4 korda päevas. Tugev positiivne soovitus, väga madal tõendatuse aste |
| 32 |
|
2. tüüpi diabeedi diagnoosiga patsiendile, kes on insuliini mitmesüsteravil, soovitage vere glükoosisisalduse kontrollimist glükomeetriga 3–4 korda päevas (nt enne põhitoidukordi ja magamaminekut). Tugev positiivne soovitus, väga madal tõendatuse ast |
33 |
|
2. tüüpi diabeedi diagnoosiga patsiendile, kes on insuliinravil, õpetage koos vere glükoosisisalduse enesemonitooringuga glükoosi näidu järgi insuliini annuse korrigeerimist. Praktiline soovitus |
Töörühm arvestas soovitust sõnastades, et igapäevane vere glükoosisisalduse kontrollimine on vajalik eelkõige intensiivsel insuliinraviskeemil olevatel patsientidel. Soovituse tugevuse suurendamisel võeti arvesse insuliinide toimeaega. Nii tehniliselt kui ka praktiliselt on intensiivsel insuliinraviskeemil olevaid patsiente teistest süsteravil olevatest patsientidest raske eristada. Seega on reaalne, et suurema glükomeetri tarvikute limiidi saavad kõik süsteravil olevad patsiendid. Kuna aga vere glükoosisisalduse mõõtmine sõrmeotsast on valulik ja ebameeldiv, on vähetõenäoline, et inimesed, kes ei pea iga päev vere glükoosisisaldust mõõtma, hakkaksid suuremat tarvikute arvu kuritarvitama, et teha lisamõõtmisi. Koos vere glükoosisisalduse mõõtmisega tuleb insuliinravil olevale patsiendile õpetada, kuidas väärtusele reageerida (sh hüpoglükeemia ravi, hüperglükeemia korrigeerimine, süsivesikute portsjoni järgi kiiretoimelise insuliini annuse arvutamine).
Vaata lähemalt kliinilise küsimuse nr 12 soovituse TõKo ja SoKo tabelit.
Patsiendi suunamine eriarstiabisse
| 34 |
|
2. tüüpi diabeedi diagnoosiga patsient, kellel on dekompenseerunud diabeet või vajalik alustada insuliinravi, kaaluge endokrinoloogi vastuvõtule suunamist. Praktiline soovitus |
| 35 |
|
2. tüüpi diabeedi diagnoosiga patsient, kellel kahtlustate muud spetsiifilist diabeedi vormi, suunake endokrinoloogi vastuvõtule Praktiline soovitus |
| 36 | |
2. tüüpi diabeedi diagnoosiga insuliinravil olev patsient suunake vähemalt üks kord aastas diabeediõe vastuvõtule. Praktiline soovitus |
| 37 |
|
2. tüüpi diabeedi diagnoosiga patsient, kes vajab spetsiifilist eluviisinõustamist (sh senine nõustamine olnud vähetõhus, esinevad kaasuvad haigused nt podagra, krooniline neerupuudulikkus, hüperkolesteroleemia, tsöliaakia jt), suunake diabeediõe või toitumisterapeudi vastuvõtule. Praktiline soovitus |
| 38 |
|
2. tüüpi diabeedi diagnoosiga patsiendil, kes on kehamassiindeksiga vähemalt 35 kg/m2, kaaluge ravijuhendi „Bariaatrilise patsiendi käsitlus enne ja pärast kirurgilist sekkumist“ põhjal üldkirurgi vastuvõtule suunamist. Praktiline soovitus |
| 39 |
|
2. tüüpi diabeedi diagnoosiga patsient, kes planeerib rasedust, suunake endokrinoloogi, naistearsti või rasedatega tegeleva sisearsti konsultatsioonile. Praktiline soovitus |
| 40 |
|
2. tüüpi diabeedi diagnoosiga patsient, kes on rasestunud, suunake endokrinoloogi, naistearsti või rasedatega tegeleva sisearsti konsultatsioonile ühe nädala jooksul. Praktiline soovitus |
Lisad
Lisa 1. 2. tüüpi diabeedi ravi algoritm
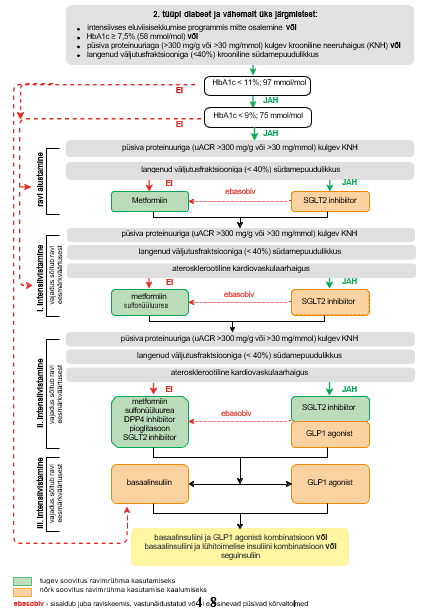

Lisa 2. Insuliinravi alustamise algoritm
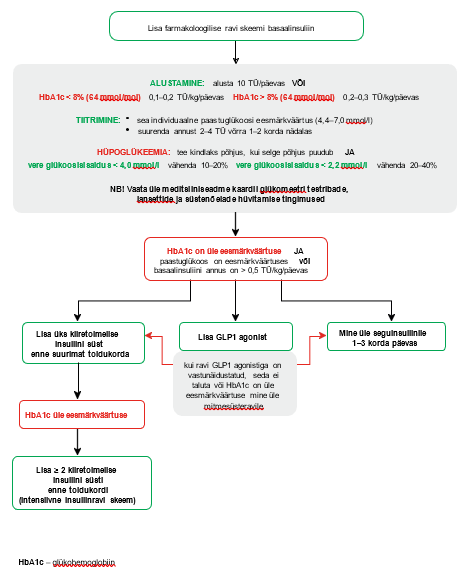
Lisa 3. 2. tüüpi diabeedi ravimid ja nende manustamine


| Ravi alustamine | Tiitrimine | Süstevahend | Kommentaar | |
| Kord päevas manustatavad GLP-1 agonistid | ||||
| Liraglutiid | 0,6 mg päevas | Alates 8. päevast 1,2 mg (tavaannus) Alates 15. päevast 1,8 mg |
Erinevate annuste jaoks sama süstal | Üks kord päevas, mis tahes kellaajal, sõltumata söögikordadest Vastunäidustatud kui eGFR alla 15 ml/ min/1,73m2 |
| Liksisenatiid | 10 mg päevas | Alates 15. päevast 20 mg päevas | Erinevate annuste jaoks erinev süstal | Üks kord päevas mis tahes söögikorrale eelneva tunni vältel Vastunäidustatud kui eGFR alla 30 ml/ min/1,73m2 |
| Semaglutiid (suukaudne) |
3 mg päevas |
Alates 2. kuust suurendada 7 mg-ni päevas (tavaannus). Alates 3. kuust võib suurendada ühe 14 mg tabletini päevas |
Tuleb võtta tühja kõhuga. Tablett tuleb alla neelata tervelt koos vähese veega (kuni 120 ml) Pärast ravimi manustamist peab patsient ootama enne söömist, joomist või teiste suukaudsete ravimite manustamist vähemalt 30 minutit Vastunäidustatud kui eGFR alla 15 ml/ min/1,73m2 |
|
| Ravi alustamine | Tiitrimine | Süstevahend | Kommentaar | |
| Kord nädalas manustatavad GLP-1 agonistid | ||||
| Eksenatiid | 2 mg nädalas | Ei tiitrita | Ühekordne süstal | Üks kord nädalas, samal päeval, sõltumata söögikordadest Vastunäidustatud kui eGFR alla 30 ml/ min/1,73m2 |
| Dulaglutiid | 1,5 mg nädalas | Ei tiitrita | Ühekordne süstal | Üks kord nädalas, samal päeval, sõltumata söögikordadest Vastunäidustatud kui eGFR alla 15 ml/ min/1,73m2 |
| Semaglutiid | 0,25 mg nädalas | Alates 5. nädalast 0,5 mg (tavaannus) Alates 9. nädalast 1,0 mg |
Erinevate annuste jaoks erinev süstal | Üks kord nädalas, samal päeval, sõltumata söögikordadest Vastunäidustatud kui eGFR alla 15 ml/ min/1,73m2 |

| Annustamise sagedus | Toime algus | Toime kestus | ||
| Basaalinsuliinid | ||||
| Detemir-insuliin | 100 TÜ/ml | 1–2 korda päevas | – | 12–20 tundi |
| Glargiin-insuliin | 100 TÜ/ml | 1 kord päevas | 24 tundi | |
| Glargiin-insuliin | 300 TÜ/ml | 1 kord päevas | 24–36 tundi | |
| Degludek-insuliin | 100 TÜ/ml 200 TÜ/ml |
1 kord päevas | > 42 tundi | |
| Seguinsuliinid | ||||
| Aspartinsuliin/ protamiiniga kristalliseeritud aspartinsuliin | 30/70% | Tavaliselt 2 korda päevas |
10–20 minutit | < 24 tundi |
| Lisproinsuliin/ protamiiniga kristalliseeritud lisproinsuliin | 25/75% | Tavaliselt 2 korda päevas |
||
| Lisproinsuliin/ protamiiniga kristalliseeritud lisproinsuliin | 50/50% | Tavaliselt 2 korda päevas |
||
| aspart-insuliin/ degludek-insuliin | 30/70% | Tavaliselt 1–2 korda päevas | > 42 tundi | |
| Lühitoimelised insuliinid | ||||
| Aspart | 100 TÜ/ml | Tavaliselt 1–3 korda päevas enne söögikordi | 10–20 minutit | 3–6 tundi |
| Lisproinsuliin | 100 TÜ/ml 200 TÜ/ml |
|||
| Glulisiin | 100 TÜ/ml | |||
| Kiiretoimeline aspartinsuliin | 100 TÜ/ml | 5–15 minutit | ||
| Kiiretoimeline lisproinsuliin | 100 TÜ/ml | |||
Lisa 4. 2. tüüpi diabeedi diagnoosiga patsiendi jälgimine
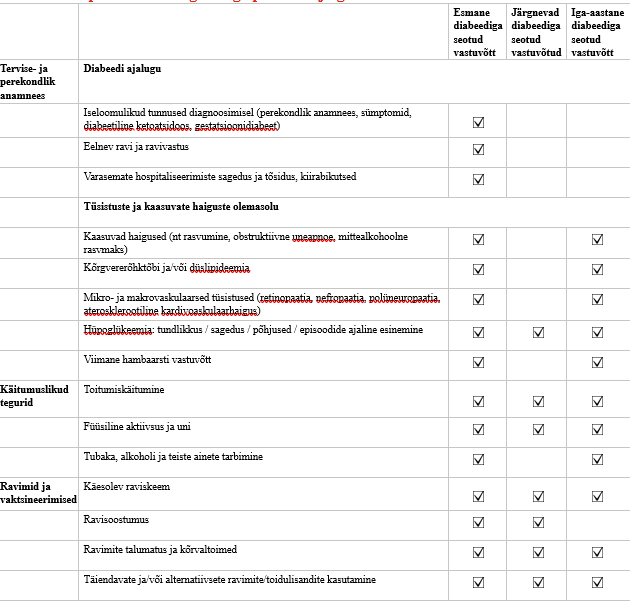

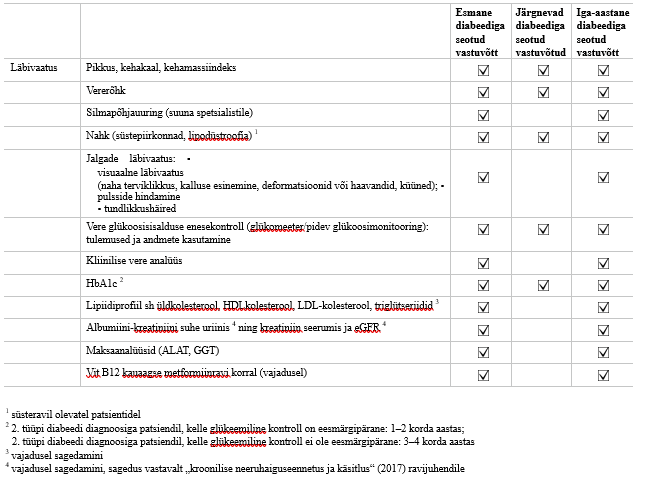
Kasutatud kirjandus
- Ambos A, Raie E, Kiudma T, Reppo I, Rätsep A, Tammiksaar K, et al. 2. tüüpi diabeedi Eesti ravijuhend 2016. Eesti Arst 2016; 95: 465–73.
- American Diabetes Association. Standards of Medical Care in Diabetes – 2021. Diabetes Care 2020; 44: S1–S232.
- Lepiksoo M, Lember M, Kull M, Kallikorm R, Rajasalu T, Vilimaa T. Suhkrutõve levimus Eesti täiskasvanud rahvastikus. Eesti Arst 2008; 87(5): 337–41.
- Eglit T, Rajasalu T, Lember M. Prevalence of diabetes and impaired glucose regulation in Estonia. Diabet Med 2011; 28: 504–5.
- International Diabetes Federation. IDF Diabetes Atlas, 9th edition. Belgium, Brussels: International Diabetes Federation; 2019.
- Tervisestatistika ja Terviseuuringute Andmebaas. EH12: Esmashaigestumus 100 000 elaniku kohta soo ja vanuserühma järgi. Tallinn: Tervise Arengu Instituut; 2020.
- Eesti Haigekassa. Eesti Haigekassa Raviarvete andmebaas. Tallinn: Eesti Haigekassa; 2021.
- SA Tartu Ülikooli Kliinikum. Ühendlabori käsiraamat: glükoos. Tartu: SA Tartu Ülikooli Kliinikum; 2021 (uuendatud).
- World Health Organization. Definition and diagnosis of diabetes mellitus and intermediate hyperglycaemia. Report of a WHO/IDF consultation. World Health Organization; 2006.
- International Expert Committee. International Expert Committee report on the role of the A1C assay in the diagnosis of diabetes. Diabetes Care 2009; 32: 1327–34.
- Estonian Health Insurance Fund. Estonian Handbook of Guidelines Development 2020. Tallinn: Estonian Health Insurance Fund; 2021.
- Xu XY, Leung AYM, Smith R, Wong JYH, Chau PH, Fong DYT. The relative risk of developing type 2 diabetes among individuals with prediabetes compared with individuals with normoglycaemia: Meta- analysis and meta-regression. J Adv Nurs 2020; 76: 3329–45.
- Ravijuhendi töörühm. Ülekaalulise või rasvunud patsiendi käsitlus esmatasandil. Ravijuhendite Nõukoda; 2019.
- Knowler WC, Barrett-Connor E, Fowler SE, Hamman RF, Lachin JM, Walker EA, et al. Reduction in the incidence of type 2 diabetes with lifestyle intervention or metformin. N Engl J Med 2002; 346: 393–403.
- Lindström J, Ilanne-Parikka P, Peltonen M, Aunola S, Eriksson JG, Hemiö K, et al. Sustained reduction in the incidence of type 2 diabetes by lifestyle intervention: follow-up of the Finnish Diabetes Prevention Study. Lancet 2006; 368:1673–9.
- Li G, Zhang P, Wang J, An Y, Gong Q, Gregg EW, et al. Cardiovascular mortality, all-cause mortality, and diabetes incidence after lifestyle intervention for people with impaired glucose tolerance in the Da Qing Diabetes Prevention Study: a 23-year follow-up study. Lancet Diabetes Endocrinol 2014; 2: 474–80.
- Madsen KS, Chi Y, Metzendorf MI, Richter B, Hemmingsen B. Metformin for prevention or delay of type 2 diabetes mellitus and its associated complications in persons at increased risk for the development of type 2 diabetes mellitus. Cochrane Database Syst Rev 2019; 12: CD008558.
- Hemmingsen B, Sonne DP, Metzendorf MI, Richter B. Insulin secretagogues for prevention or delay of type 2 diabetes mellitus and its associated complications in persons at increased risk for the development of type 2 diabetes mellitus. Cochrane Database Syst Rev 2016; 10: CD012151.
- Hemmingsen B, Gimenez-Perez G, Mauricio D, Roqué i Figuls M, Metzendorf MI, Richter B. Diet, physical activity or both for prevention or delay of type 2 diabetes mellitus and its associated complications in people at increased risk of developing type 2 diabetes mellitus. Cochrane Database Syst Rev 2017; 12: CD003054.
- Haw JS, Galaviz KI, Straus AN, Kowalski AJ, Magee MJ, Beth Weber M. Long-term Sustainability of Diabetes Prevention Approaches. A Systematic Review and Meta-analysis of Randomized Clinical Trials. JAMA Intern Med 2017; 177: 1808–17.
- Sheng Z, Cao JY, Pang YC, Xu HC, Chen JW, Yuan JH, et al. Effects of Lifestyle Modification and Anti-diabetic Medicine on Prediabetes Progress: A Systematic Review and Meta-Analysis. Front Endocrinol 2019; 10: 455.
- Gonzalez-Heredia T, Hernandez-Corona DM, Gonzalez-Ortiz M, Martınez- Abundis E. Effect of Linagliptin Versus Metformin on Glycemic Variability in Patients with Impaired Glucose Tolerance. Diabetes Technol Ther 2017; 19: 471–475.
- Inzucchi SE, Viscoli CM, Young LH, Furie KL, Gorman M, Lovejoy AM, et al. Pioglitazone Prevents Diabetes in Patients With Insulin Resistance and Cerebrovascular Disease. Diabetes Care 2016; 39: 1684–92.
- Hamdy O, Mottalib A, Morsi A, El-Sayed N, Goebel-Fabbri A, Arathuzik G, et al. Long-term effect of intensive lifestyle intervention on cardiovascular risk factors in patients with diabetes in real-world clinical practice: a 5-year longitudinal study. BMJ Open Diabetes Res Care 2017; 5: e000259.
- National Institute for Health and Care Excellence. Type 2 diabetes in adults: management. England: National Institute for Health and Care Excellence; 2019 (updated).
- Scottish Intercollegiate Guidelines Network. Pharmacological management of glycaemic control in people with type 2 diabetes. Scotland: Scottish Intercollegiate Guidelines Network; 2017.
- European Society of Cardiology and European Association for the Study of Diabetes. 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed incollaboration with the EASD. Eur Heart J 2020; 41: 255–323.
- American Association of Clinical Endocrinologists and American College of Endocrinology. Consensus statement by the American Association of Clinical Endocrinologists and American College of Endocrinology on the comprehensive type 2 diabetes management algorithm – 2020 executive summary. Endocr Pract 2020; 26: 107–39.
- Franz MJ, Boucher JL, Rutten-Ramos S, Van Wormer JJ. Lifestyle weight- loss intervention outcomes in overweight and obese adults with type 2 diabetes: a systematic review and metaanalysis of randomized clinical trials. J Acad Nutr Diet 2015; 115: 1447–63.
- Medical Advisory Secretariat. Behavioural interventions for type 2 diabetes: an evidence-based analysis. Ont Health Technol Assess Ser 2009; 9: 1–45.
- Umpierre D, Ribeiro PA, Kramer CK, Leitao CB, Zucatti AT, Azevedo MJ,et al. Physical activity advice only or structured exercise training and association with HbA1c levels in type 2 diabetes: a systematic review and meta-analysis. JAMA 2011; 305: 1790–9.
- Cradock KA, Ć Laighin G, Finucane FM, McKay R, Quinlan LR, Martin Ginis KA, et al. Diet Behavior Change Techniques in Type 2 Diabetes: A Systematic Review and Meta-analysis. Diabetes Care 2017; 40: 1800–10.
- Gnesin F, Thuesen ACB, Kähler LKA, Madsbad S, Hemmingsen B. Metformin monotherapy for adults with type 2 diabetes mellitus. Cochrane Database Syst Rev 2020; 6:CD012906.
- Tsapas A, Avgerinos I, Karagiannis T, Malandris K, Manolopoulos A, Andreadis P, et al. Comparative Effectiveness of Glucose-Lowering Drugs for Type 2 Diabetes: A Systematic Review and Network Meta-analysis. Ann Intern Med 2020; 173: 278–86.
- World Health Organization. Guidelines on second-and third-line medicines and type of insulin for the control of blood glucose levels in non-pregnant adults with diabetes mellitus. World Health Organization; 2018.
- Emerging Risk Factors Collaboration, Sarwar N, Gao P, Seshasai SR, Gobin R, Kaptoge S, et al. Diabetes mellitus, fasting blood glucose concentration, and risk of vascular disease: a collaborative meta-analysis of 102 prospective studies. Lancet 2010; 375: 2215–22.
- Zinman B, Wanner C, Lachin JM, Fitchett D, Bluhmki E, Hantel S, et al. Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes. N Engl J Med 2015; 373: 2117–28.
- Neal B, Perkovic V, Mahaffey KW, de Zeeuw D, Fulcher G, Erondu N, et al. Canagliflozin and Cardiovascular and Renal Events in Type 2 Diabetes. N Engl J Med 2017; 377: 644–57.
- Wiviott SD, Raz I, Bonaca MP, Mosenzon O, Kato E, Cahn A, et al. Dapagliflozin and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med. 2019; 380: 347–57.
- Perkovic V, Jardine MJ, Neal B, Bompoint S, Heerspink HJL, Charytan DM, et al. Canagliflozin and Renal Outcomes in Type 2 Diabetes and Nephropathy. N Engl J Med 2019; 380: 2295–2306.
- Cannon CP, Pratley R, Dagogo-Jack S, Mancuso J, Huyck S, Masiukiewicz U, et al. Cardiovascular Outcomes with Ertugliflozin in Type 2 Diabetes. N Engl J Med 2020; 383: 1425–35.
- McMurray JJV, Solomon SD, Inzucchi SE, Køber L, Kosiborod MN, Martinez FA, et al. Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction. N Engl J Med 2019; 381: 1995–2008.
- Packer M, Anker SD, Butler J, Filippatos G, Pocock SJ, Carson P, et al. Cardiovascular and Renal Outcomes with Empagliflozin in Heart Failure. N Engl J Med 2020; 383: 1413–24.
- Heerspink HJL, Stefánsson BV, Correa-Rotter R, Chertow GM, Greene T, Hou FF, et al. Dapagliflozin in Patients with Chronic Kidney Disease. N Engl J Med 2020; 383: 1436–46.
- Bhatt DL, Szarek M, Steg PG, Cannon CP, Leiter LA, McGuire DK, et al. Sotagliflozin in Patients with Diabetes and Recent Worsening Heart Failure. N Engl J Med 2021; 384: 117–28.
- Bhatt DL, Szarek M, Pitt B, Cannon CP, Leiter LA, McGuire DK, et al. Sotagliflozin in Patients with Diabetes and Chronic Kidney Disease. N Engl J Med 2021; 384: 129–39.
- Pfeffer MA, Claggett B, Diaz R, Dickstein K, Gerstein HC, Køber LV, et al. Lixisenatide in Patients with Type 2 Diabetes and Acute Coronary Syndrome. N Engl J Med 2015; 373: 2247–57.
- Marso SP, Daniels GH, Brown-Frandsen K, Kristensen P, Mann JFE, Nauck MA, et al. Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med 2016; 375: 311–22.
- Marso SP, Bain SC, Consoli A, Eliaschewitz FG, Jódar E, Leiter LA, et al. Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. N Engl J Med 2016; 375: 1834–44.
- Holman RR, Bethel MA, Mentz RJ, Thompson VP, Lokhnygina YB, John BC, et al. Effects of Once-Weekly Exenatide on Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med 2017; 377: 1228–39.
- Hernandez AF, Green JB, Janmohamed S, D’Agostino RB, Granger CB, Jones NP, et al. Albiglutide and cardiovascular outcomes in patients with type 2 diabetes and cardiovascular disease (Harmony Outcomes): a double- blind, randomised placebo-controlled trial. Lancet 2018; 392: 1519–29.
- Gerstein HC, Colhoun HM, Dagenais GR, Diaz R, Lakshmanan M, Pais P, et al. Dulaglutide and cardiovascular outcomes in type 2 diabetes (REWIND): a double-blind, randomised placebo-controlled trial. Lancet 2019; 394: 121–30.
- Husain M, Birkenfeld AL, Donsmark M, Dungan K, Eliaschewitz FG, Franco DR, et al. Oral Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. N Engl J Med 2019; 381: 841–51.
- Ida S, Kaneko R, Murata K. Effects of oral antidiabetic drugs on left ventricular mass in patients with type 2 diabetes mellitus: a network meta- analysis. Cardiovasc Diabetol 2018; 17: 129.
- Lee G, Oh SW, Hwang SS, Yoon JW, Kang S, Joh HK, et al. Comparative effectiveness of oral antidiabetic drugs in preventing cardiovascular mortality and morbidity: A network meta-analysis. PLoS One 2017; 12: e0177646.
- Griffin SJ, Leaver JK, Irving GJ. Impact of metformin on cardiovascular disease: a meta-analysis of randomised trials among people with type 2 diabetes. Diabetologia 2017; 60: 1620–29.
- Monami M, Genovese S, Mannucci E. Cardiovascular safety of sulfonylureas: a meta-analysis of randomized clinical trials. Diabetes Obes Metab 2013; 15: 938–53.
- Grenet G, Ribault S, Nguyen GB, Glais F, Metge A, Linet T, et al. GLUcose COntrol Safety & Efficacy in type 2 DIabetes, a systematic review and NETwork meta-analysis. PLoS One 2019; 14: e0217701.
- Han Y, Xie H, Liu Y, Gao P, Yang X, Shen Z. Effect of metformin on allcause and cardiovascular mortality in patients with coronary artery diseases: a systematic review and an updated meta-analysis. Cardiovasc Diabetol 2019; 18: 96.
- Pladevall M, Riera-Guardia N, Margulis AV, Varas-Lorenzo C, Calingaert B, Perez-Gutthann S. Cardiovascular risk associated with the use of glitazones, metformin and sufonylureas: meta-analysis of published observational studies. BMC Cardiovasc Disord 2016; 16: 14.
- Scheller NM, Mogensen UM, Andersson C, Vaag A, Torp-Pedersen C. All-cause mortality and cardiovascular effects associated with the DPP-IV inhibitor sitagliptin compared with metformin, a retrospective cohort study on the Danish population. Diabetes Obes Metab 2014; 16: 231–6.
- Ou HT, Chang KC, Li CY, Wu JS. Risks of cardiovascular diseases associated with dipeptidyl peptidase-4 inhibitors and other antidiabetic drugs in patients with type 2 diabetes: a nation-wide longitudinal study. Cardiovasc Diabetol 2016; 15: 41.
- Whitlock RH, Hougen I, Komenda P, Rigatto C, Clemens KK, Tangri N. A Safety Comparison of Metformin vs Sulfonylurea Initiation in Patients With Type 2 Diabetes and Chronic Kidney Disease: A Retrospective Cohort Study. Mayo Clin Proc 2020; 95: 90–100.
- Lambadiari V, Pavlidis G, Kousathana F, Varoudi M, Vlastos D, Maratou E, et al. Effects of 6-month treatment with the glucagon like peptide-1 analogue liraglutide on arterial stiffness, left ventricular myocardial deformation and oxidative stress in subjects with newly diagnosed type 2 diabetes. Cardiovasc Diabetol 2018; 17: 8.
- McGuire DK, Shih WJ, Cosentino F, Charbonnel B, Cherney DZI, Dagogo- Jack S, et al. Association of SGLT2 Inhibitors With Cardiovascular and Kidney Outcomes in Patients With Type 2 Diabetes: A Meta-analysis. JAMA Cardiol 2021; 6: 148–58.
- Palmer SC, Tendal B, Mustafa RA, Vandvik PO, Li S, Hao Q, et al. Sodium-glucose cotransporter protein-2 (SGLT-2) inhibitors and glucagon- like peptide-1 (GLP-1) receptor agonists for type 2 diabetes: systematic review and network meta-analysis of randomised controlled trials. BMJ 2021; 372: m4573.
- Chen Z, Li G. Sodium-Glucose Co-Transporter 2 Inhibitors Compared with Sulfonylureas in Patients with Type 2 Diabetes Inadequately Controlled on Metformin: A Meta-Analysis of Randomized Controlled Trials. Clin Drug Investig 2019; 39: 521–31.
- Mishriky BM, Tanenberg RJ, Sewell KA, Cummings DM. Comparing SGLT-2 inhibitors to DPP-4 inhibitors as an add-on therapy to metformin in patients with type 2 diabetes: A systematic review and meta-analysis. Diabetes Metab 2018; 44: 112–20.
- Mishriky BM, Cummings DM, Tanenberg RJ. The efficacy and safety of DPP4 inhibitors compared to sulfonylureas as add-on therapy to metformin in patients with Type 2 diabetes: A systematic review and meta-analysis. Diabetes Res Clin Pract 2015; 109: 378–88.
- Farah D, Leme GM, Eliaschewitz FG, Fonseca MCM. A safety and tolerability profile comparison between dipeptidyl peptidase-4 inhibitors and sulfonylureas in diabetic patients: A systematic review and meta- analysis. Diabetes Res Clin Pract 2019; 149: 47–63.
- Li M, Yang Y, Jiang D, Ying M, Wang Y, Zhao R. Efficacy and safety of liraglutide versus sitagliptin both in combination with metformin in patients with type 2 diabetes: A systematic review and meta-analysis. Medicine 2017; 96: e8161.
- Peng Y, Chen SH, Liu XN, Sun QY. Efficacy of different antidiabetic drugs based on metformin in the treatment of type 2 diabetes mellitus: A network meta-analysis involving eight eligible randomized-controlled trials. J Cell Physiol 2019; 234: 2795–2806.
- Wang Z, Sun J, Han R, Fan D, Dong X, Luan Z, et al. Efficacy and safety of sodium-glucose cotransporter-2 inhibitors versus dipeptidyl peptidase-4 inhibitors as monotherapy or add-on to metformin in patients with type 2 diabetes mellitus: A systematic review and meta-analysis. Diabetes Obes Metab 2018; 20: 113–120.
- Goring S, Hawkins N, Wygant G, Roudaut M, Townsend R, Wood I, et al. Dapagliflozin compared with other oral anti-diabetes treatments when added to metformin monotherapy: a systematic review and network meta- analysis. Diabetes Obes Metab 2014; 16: 433–42.
- Liu SC, Tu YK, Chien MN, Chien KL. Effect of antidiabetic agents added to metformin on glycaemic control, hypoglycaemia and weight change in patients with type 2 diabetes: a network meta-analysis. Diabetes Obes Metab 2012; 14: 810–20.
- Palmer SC, Mavridis D, Nicolucci A, Johnson DW, Tonelli M, Craig JC, et al. Comparison of Clinical Outcomes and Adverse Events Associated With Glucose-Lowering Drugs in Patients With Type 2 Diabetes: A Meta- analysis. JAMA 2016; 316: 313–24.
- Qian D, Zhang T, Tan X, Zhen P, Liang Z, Xie J, et al. Comparison of antidiabetic drugs added to sulfonylurea monotherapy in patients with type 2 diabetes mellitus: A network meta-analysis. PLoS One 2018; 13: e0202563.
- Yoon JH, Min SH, Ahn CH, Cho YM, Hahn S. Comparison of non-insulin antidiabetic agents as an add-on drug to insulin therapy in type 2 diabetes: a network meta-analysis. Sci Rep 2018; 8: 4095.
- Zaccardi F, Dhalwani NN, Dales J, Mani H, Khunti K, Davies MJ, et al. Comparison of glucose-lowering agents after dual therapy failure in type 2 diabetes: A systematic review and network meta-analysis of randomized controlled trials. Diabetes Obes Metab 2018; 20: 985–97.
- McIntosh B, Cameron C, Singh SR, Yu C, Dolovich L, Houlden R. Choice of therapy in patients with type 2 diabetes inadequately controlled with metformin and a sulphonylurea: a systematic review and mixed-treatment comparison meta-analysis. Open Med 2012; 6: e62–74.
- Gross JL, Kramer CK, Leitão CB, Hawkins N, Viana LV, Schaan BD, et al. Effect of antihyperglycemic agents added to metformin and a sulfonylurea on glycemic control and weight gain in type 2 diabetes: a network meta- analysis. Ann Intern Med 2011; 154: 672–9.
- Goudswaard AN, Furlong NJ, Rutten GE, Stolk RP, Valk GD. Insulin monotherapy versus combinations of insulin with oral hypoglycaemic agents in patients with type 2 diabetes mellitus. Cochrane Database Syst Rev 2004; 4: CD003418.
- Vos RC, van Avendonk MJ, Jansen H, Goudswaard AN, van den Donk M, Gorter K, et al. Insulin monotherapy compared with the addition of oral glucose-lowering agents to insulin for people with type 2 diabetes already on insulin therapy and inadequate glycaemic control. Cochrane Database Syst Rev 2016; 9: CD006992.
- ORIGIN Trial Investigators. Predictors of nonsevere and severe hypoglycemia during glucose-lowering treatment with insulin glargine or standard drugs in the ORIGIN trial. Diabetes Care 2015; 38: 22–8.
- Gerich JE. Role of the kidney in normal glucose homeostasis and in the hyperglycaemia of diabetes mellitus: therapeutic implications. Diabet Med 2010; 27: 136–42.
- Seppet E. Neer uudsete diabeediravimite – SGLT2 inhibiitorite – sihtmärgina. Eesti Arst 2014; 93: 599.
- Zannad F, Ferreira JP, Pocock SJ, Anker SD, Butler J, Filippatos G, et al. SGLT2 inhibitors in patients with heart failure with reduced ejection fraction: a meta-analysis of the EMPEROR-Reduced and DAPA-HF trials. Lancet 2020; 396: 819–829.
- Neuen BL, Arnott C, Perkovic V, Figtree G, de Zeeuw D, Fulcher G, et al. Sodium-glucose co-transporter-2 inhibitors with and without metformin: A meta-analysis of cardiovascular, kidney and mortality outcomes. Diabetes Obes Metab 2021; 23: 382–390.
- Heyward J, Mansour O, Olson L, Singh S, Alexander GC. Association between sodium-glucose cotransporter 2 (SGLT2) inhibitors and lower extremity amputation: A systematic review and meta-analysis. PLoS One 2020; 15: e0234065.
- Puckrin R, Saltiel MP, Reynier P, Azoulay L, Yu OHY, Filion KB. SGLT-2 inhibitors and the risk of infections: a systematic review and meta-analysis of randomized controlled trials. Acta Diabetol 2018; 55: 503–14.
- Toyama T, Neuen BL, Jun M, Ohkuma T, Neal B, Jardine MJ, et al. Effect of SGLT2 inhibitors on cardiovascular, renal and safety outcomes in patients with type 2 diabetes mellitus and chronic kidney disease: A systematic review and meta-analysis. Diabetes Obes Metab 2019; 21: 1237–50.
- Li J, Gong Y, Li C, Lu Y, Liu Y, Shao Y. Long-term efficacy and safety of sodium-glucose cotransporter-2 inhibitors as add-on to metformin treatment in the management of type 2 diabetes mellitus: A meta-analysis.Medicine 2017; 96: e7201.
- Kawalec P, Mikrut A, Łopuch S. The safety of dipeptidyl peptidase-4 (DPP-4) inhibitors or sodium-glucose cotransporter 2 (SGLT-2) inhibitors added to metformin background therapy in patients with type 2 diabetes mellitus: a systematic review and meta-analysis. Diabetes Metab Res Rev 2014; 30: 269–83.
- Figueiredo IR, Rose SCP, Freire NB, Patrocínio MS, Pierdoná N, Bittencourt RJ. Use of sodium-glucose cotransporter-2 inhibitors and urinary tract infections in type 2 diabetes patients: a systematic review. Rev Assoc Med Bras 2019; 65: 246–52.
- Monami M, Nreu B, Zannoni S, Lualdi C, Mannucci E. Effects of SGLT- 2 inhibitors on diabetic ketoacidosis: A meta-analysis of randomised controlled trials. Diabetes Res Clin Pract 2017; 130: 53–60.
- SA Tartu Ülikooli Kliinikum. Ühendlabori käsiraamat: glükohemoblobiin. Tartu: SA Tartu Ülikooli Kliinikum; 2021.
- Hasan R, Firwana B, Elraiyah T, Domecq JP, Prutsky G, Nabhan M, et al. A systematic review and meta-analysis of glycemic control for the prevention of diabetic foot syndrome. J Vasc Surg 2016; 63: 22S–28S.
- Herrera-Gómez F, Asensio-González M, González-López A ,Álvarez FJ. Effects of Intensive Control of Glycemia on Clinical Kidney Outcomes in Type 2 Diabetes Patients Compared with Standard Control: A Meta- Analysis. Front Pharmacol 2017; 8: 845.
- Hemmingsen B, Lund SS, Gluud C, Vaag A, Almdal TP, Hemmingsen C, et al. Targeting intensive glycaemic control versus targeting conventional glycaemic control for type 2 diabetes mellitus. Cochrane Database Syst Rev 2013; 11: CD008143.
- American Diabetes Association. Standards of Medical Care in Diabetes 2014. Diabetes Care 2014; 37: S14–S80.
- International Diabetes Federation/SMBG International Working Group. IDF guideline on self-monitoring of blood glucose in non-insulin treated type 2 diabetes. Belgium, Brussels: International Diabetes Federation; 2012.
- Ceriello A, Barkai L, Christiansen JS, Czupryniak L, Gomis R, Harno K, et al. Diabetes as a case study of chronic disease management with a personalized approach: the role of a structured feedback loop. Diabetes Res Clin Pract 2012; 98: 5–10.
- Raz I, Hauser E, Bursztyn M. Moderate exercise improves glucose metabolism in uncontrolled elderly patients with non-insulin-dependent diabetes mellitus. Isr J Med Sci 1994; 30: 766–70.
- International Diabetes Federation Guideline Development Group. Guideline for management of postmeal glucose in diabetes. Diabetes Res Clin Pract 2014; 103: 256–68.
- American Association of Diabetes Educators. AADE Position Statement. Diabetes Educ 2006; 32: 835–6, 844–7.
- Americal Diabetes Association. Standards of Medical Care in Diabetes 2020. Diabetes Care 2020; 43: S1–S212.
- Mannucci E, Antenore A, Giorgino F, Scavini M. Effects of Structured Versus Unstructured Self-Monitoring of Blood Glucose on Glucose Control in Patients With Non-insulin-treated Type 2 Diabetes: A Meta-Analysis of Randomized Controlled Trials. J Diabetes Sci Technol 2018; 12: 183–9.
- Malanda UL, Welschen LMC, Riphagen II, Dekker JM, Nijpels G, Bot SDM. Self-monitoring of blood glucose in patients with type 2 diabetes mellitus who are not using insulin. Cochrane Database Syst Rev 2012; 1: CD005060.
- Sarol JN Jr, Nicodemus NA Jr, Tan KM, Grava MB. Self-monitoring of blood glucose as part of a multi-component therapy among non-insulin requiring type 2 diabetes patients: a meta-analysis (1966–2004). Curr Med Res Opin 2005; 21: 173–84.
- Xu Y, Tan DHY, Lee JY. Evaluating the impact of self‐monitoring of blood glucose frequencies on glucose control in patients with type 2 diabetes who do not use insulin: A systematic review and meta‐analysis. Int J Clin Pract 2019; 73: e13357.
- Hongmei Z, Yanan Z, Siu-wai L. Is self-monitoring of blood glucose effective in improving glycaemic control in type 2 diabetes without insulin treatment: a meta-analysis of randomised controlled trials. BMJ Open 2016; 6: e010524.
- Machry RV, Rados DV, Gregório GR, Rodrigues TC. Self-monitoring blood glucose improves glycemic control in type 2 diabetes without intensive treatment: A systematic review and meta-analysis. Diabetes Res Clin Pract 2018; 142: 173–87.
- Farmer A, Wade A, Goyder E, Yudkin P, French D, Craven A, et al. Impact of self monitoring of blood glucose in the management of patients with non-insulin treated diabetes: open parallel group randomised trial. BMJ 2007; 335: 132.
- Young LA, Buse JB, Weaver MA, Vu MB, Mitchell CM, Blakeney T, et al. Glucose Self-monitoring in Non–Insulin-Treated Patients With Type 2 Diabetes in Primary Care Settings: A Randomized Trial. JAMA Intern Med 2017; 177: 920–29.
- Polonsky WH, Fisher L, Schikman CH, Hinnen DA, Parkin CG, Jelsovsky Z, Petersen B, Schweitzer M, Wagner RS. Structured self-monitoring of blood glucose significantly reduces A1C levels in poorly controlled, noninsulin-treated type 2 diabetes: results from the Structured Testing Program study. Diabetes Care 2011; 34: 262–7.
- Moreland EC, Volkening LK, Lawlor MT, Chalmers KA, Anderson BJ, Laffel LM. Use of a Blood Glucose Monitoring Manual to Enhance Monitoring Adherence in Adults With Diabetes: A Randomized Controlled Trial. Arch Intern Med 2006; 166: 689–95.
- Nishimura A, Harashima S, Fujita Y, Tanaka D, Wang Y, Liu Y, et al. Effects of structured testing versus routine testing of blood glucose in diabetes self-management: A randomized controlled trial. J Diabetes Complications 2017; 31: 228–33.
- Li CL, Wu YC, Kornelius E, Chen YJ, Lin YT, Hsiao HW, et al. Comparison of Different Models of Structured Self-Monitoring of Blood Glucose in Type 2 Diabetes. Diabetes Technol Ther 2016; 18: 171–7.
- O’Kane MJ, Bunting B, Copeland M, Coates VE. Efficacy of self monitoring of blood glucose in patients with newly diagnosed type 2 diabetes (ESMON study): randomised controlled trial. BMJ 2008; 336: 1174–7.
- Simon J, Gray A, Clarke P, Wade A, Neil A, Farmer A. Cost effectiveness of self monitoring of blood glucose in patients with non-insulin treated type 2 diabetes: economic evaluation of data from the DiGEM trial. BMJ 2008; 336: 1177–80.
- Farmer A, Wade A, French D, Simon J, Yudkin P, Gray A, et al. Blood glucose self-monitoring in type 2 diabetes: a randomised controlled trial. Health Technol Assess 2009; 13: 1–50.
- Aydın H, Deyneli O, Yavuz D, Tarcin Ö, Akalin S. Does the frequency of the self monitoring of blood glucose influence glycemic control in type 2 diabetic patients? Marmara Medical Journal 2005; 18; 13–16.
- Hortensius J, Kleefstra N, Landman GWD, Houweling BT, Groenier KH, van der Bijl JJ, et al. Effects of three frequencies of self-monitored blood glucose on HbA1c and quality of life in patients with type 2 diabetes with once daily insulin and stable control: a randomized trial. BMC Res Notes 2018; 11: 26.
- Lalić NM, Lalić K, Jotić A, Stanojević D, Živojinović D, Janićijević A, et al. The Impact of Structured Self-Monitoring of Blood Glucose Combined With Intensive Education on HbA1c Levels, Hospitalizations, and Quality- of-Life Parameters in Insulin-Treated Patients With Diabetes at Primary Care in Serbia: The Multicenter SPA-EDU Study. J Diabetes Sci Technol 2017; 11: 746–52.
- Gao L, Ji L, Su Q, Feng B, Shan Z, Hu R, et al. Impact of structured self- monitoring of blood glucose on the quality of life of insulin-treated Chinese patients with type 2 diabetes mellitus: Results from the COMPASS study. Diabetes Res Clin Pract 2016; 112: 88–93.
- Ji L, Su Q, Feng B, Shan Z, Hu R, Xing X, et al. Structured self-monitoring of blood glucose regimens improve glycemic control in poorly controlled Chinese patients on insulin therapy: Results from COMPASS. J Diabetes 2017; 9: 495–501.
- Soto González A, Quintela Fernández N, Pumar López A, Darias Garzón R, Rivas Fernández M, Barberá Comes G. Relationship between metabolic control and self-monitoring of blood glucose in insulin-treated patients with diabetes mellitus. Endocrinol Nutr 2015; 62: 233–9.